网址:http://m.1010jiajiao.com/timu3_id_255600[举报]
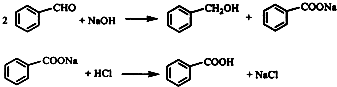
已知:
①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃).
②乙醚沸点34.6℃,密度0.7138,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸.
③石蜡油沸点高于250℃
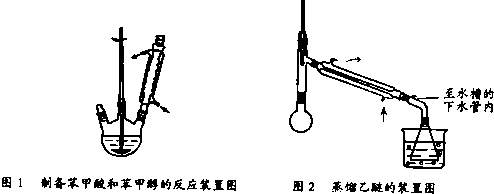
实验步骤如下:
①向图l 所示装置中加入8g氢氧化钠和30mL水,搅拌溶解.稍冷,加入10mL苯甲醛.开启搅拌器,调整转速,使搅拌平稳进行.加热回流约40min.
②停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温.反应物冷却至室温后,用乙醚萃取三次,每次
10mL.水层保留待用.合并三次萃取液,依次用5mL饱和亚硫酸氢钠溶液洗涤,10mL 10%碳酸钠溶液洗涤,10mL水洗涤,分液水层弃去所得醚层进行实验③.
③将分出的醚层,倒入干燥的锥形瓶,加无水硫酸镁,注意锥形瓶上要加塞.将锥形瓶中溶液转入图2 所示蒸馏装置,先缓缓加热,蒸出乙醚;蒸出乙醚后必需改变加热方式,升温至140℃时应对水冷凝管冷凝方法调整,继续升高温度并收集203℃~205℃的馏分得产品A.
④实验步骤②中保留待用水层慢慢地加入到盛有30mL浓盐酸和30mL水的混合物中,同时用玻璃棒搅拌,析出白色固体.冷却,抽滤,得到粗产品,然后提纯得产品B.
根据以上步骤回答下列问题:
(1)步骤②萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需
(2)饱和亚硫酸氢钠溶液洗涤是为了除去


(3)步骤③中无水硫酸镁是
(4)蒸馏除乙醚的过程中采用的加热方式为
(5)提纯产品B 所用到的实验操作为

已知:
①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃)
②乙醚沸点34.6℃,相对密度0.7138,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸.

实验步骤如下:
①向图1所示装置中加入8g氢氧化钠和30mL水,搅拌溶解.稍冷,加入10mL新蒸过的苯甲醛.开启搅拌器,调整转速,使搅拌平稳进行.加热回流约40min.
②停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温.反应物冷却至室温后,倒入分液漏斗,用乙醚萃取三次,每次10mL.水层保留待用.合并三次萃取液,依次用5mL饱和亚硫酸氢钠溶液洗涤,10mL 10%碳酸钠溶液洗涤,10mL水洗涤.
③分出醚层,倒入干燥的锥形瓶,加无水硫酸镁,注意锥形瓶上要加塞.将锥形瓶中溶液转入图2所示蒸馏装置,缓缓加热蒸馏除去乙醚.当温度升到140℃时改用空气冷凝管,收集198℃~204℃的馏分得产品A.将萃取后的水溶液慢慢地加入到盛有30mL浓盐酸和30mL水的混合物中,同时用玻璃棒搅拌,析出白色固体.冷却,过滤,得到粗产品,然后提纯得产品B.
根据以上步骤回答下列问题:
(1)步骤①中所加的苯甲醛为什么要是新蒸过的?
(2)步骤②萃取时用到的玻璃仪器有烧杯、
(3)步骤③中无水硫酸镁的作用是
(4)产品A为
(1)实验室制乙烯的化学方程式为
(2)关于该实验的说法中正确的是
a.浓硫酸只作催化剂 b.可用向下排空气法收集乙烯
c.在反应容器中放入几片碎瓷片防止混合液暴沸
d.温度计应插入反应溶液液面下,以便控制温度
(3)实验后期制得的乙烯气体中常含有杂质气体SO2和CO2,将此混合气体直接通入溴水中,若观察到溴水褪色,能否证明乙烯发生了加成反应?
实验室常用浓硫酸和乙醇混合加热制取乙烯。
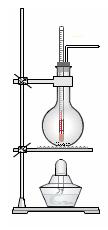
(1) 实验室制乙烯的化学方程式为 。
(2)实验室用浓硫酸和乙醇混合加热制乙烯可用如上图所示装置,下列说法正确的是 。
A.浓硫酸只作催化剂
B.在反应容器中放入几片碎瓷片防止混合液暴沸
C.反应温度缓慢上升至170℃
D.用排水法或向下排气法收集乙烯
E.园底烧瓶中装得是4mL乙醇和12mL3mol/L H2SO4混合液
F.温度计应插入反应溶液液面下,以便控制温度
G.反应完毕后先熄灭酒精灯,再从水中取出导管
(3)若将此装置中的温度计换成分液漏斗,则还可以制取的气体有(酒精灯可用可不用) 。
A.CO2 B.NH3 C.O2 D.SO2 E.NO2 F.Cl2
(4) 如温度过高,反应后溶液颜色变 。某同学设计下列实验以确定上述混合气体中含有乙烯和SO2。
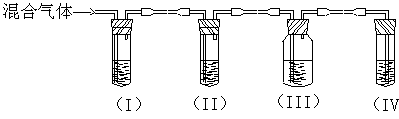
①I、II、III、IV装置可盛放的试剂是(请将下列有关试剂的序号填入空格内):
A、品红 B、NaOH溶液 C、浓硫酸 D、酸性KMnO4溶液
I ;II ;III ;IV 。
②能说明SO2气体存在的现象是
③使用装置II的目的是 ;
④使用置III的目的是 ;
⑤确定含有乙烯的现象是 。
查看习题详情和答案>>实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸,反应式如下:
已知:
①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃)。
②乙醚沸点34.6℃,密度0.7138,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸。
③石蜡油沸点高于250℃
实验步骤如下:
① 向图l 所示装置中加入8g氢氧化钠和30mL水,搅拌溶解。稍冷,加入10 mL苯甲醛。开启搅拌器,调整转速,使搅拌平稳进行。加热回流约40 min。
②停止加热,从球形冷凝管上口缓缓加入冷水20 mL,摇动均匀,冷却至室温。反应物冷却至室温后,用乙醚萃取三次,每次10 mL。水层保留待用。合并三次萃取液,依次用5 mL饱和亚硫酸氢钠溶液洗涤,10 mL 10%碳酸钠溶液洗涤,10 mL水洗涤,分液水层弃去所得醚层进行实验③。
③将分出的醚层,倒入干燥的锥形瓶,加无水硫酸镁,注意锥形瓶上要加塞。将锥形瓶中溶液转入图2 所示蒸馏装置,先缓缓加热,蒸出乙醚;蒸出乙醚后必需改变加热方式,升温至140℃时应对水冷凝管冷凝方法调整,继续升高温度并收集203℃~205℃的馏分得产品A。
④实验步骤②中保留待用水层慢慢地加入到盛有30 mL浓盐酸和30 mL水的混合物中,同时用玻璃棒搅拌,析出白色固体。冷却,抽滤,得到粗产品,然后提纯得产品B。
根据以上步骤回答下列问题:
(1)步骤②萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需 (仪器名称),实验前对该仪器进行检漏操作,方法是________________________________。
(2)饱和亚硫酸氢钠溶液洗涤是为了除去 ,而用碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸。醚层中少量的苯甲酸是从水层转移过来的,请用离子方程式说明其产生原因___________________________。
(3)步骤③中无水硫酸镁是 剂;产品A为
(4)蒸馏除乙醚的过程中采用的加热方式为 ;蒸馏得产品A加热方式是_______________;蒸馏温度高于140℃时应改用_________________冷凝。
(5)提纯产品B 所用到的实验操作为 。
查看习题详情和答案>>