摘要:配平下列化学方程式并标出电子转移方向和数目.指出氧化剂和氧化产物. (1) KMnO4 + K2SO3 + H2O - MnO2œ + K2SO4+ KOH 氧化剂 ,氧化产物 . (2) KClO3 + HCl - KCl + Cl2› + H2O 氧化剂 ,氧化产物 .
网址:http://m.1010jiajiao.com/timu3_id_255459[举报]
(1)配平下列离子方程式:
+
在反应中,若消耗Ix-与Cl2物质的量之比为1:8,则x=
(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:Mn2++S2
+H2O→Mn
+S
+H+,该反应常用于检验Mn2+的存在.其特征现象是
(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有
(4)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是
查看习题详情和答案>>
2
2
Ix-+5+x
5+x
Cl2+6x
6x
H2O---(10+2x)
(10+2x)
Cl-+2
2
I| O | - 3 |
12H+
12H+
,在反应中,若消耗Ix-与Cl2物质的量之比为1:8,则x=
11
11
.?(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:Mn2++S2
| O | 2- 8 |
| O | - 4 |
| O | 2- 4 |
溶液由无色变为紫色
溶液由无色变为紫色
,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为0.25
0.25
mol.(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有
Cl2
Cl2
.(4)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
10
10
NaBiO3+4
4
MnSO4+14
14
H2SO4-3
3
Na2SO4+5
5
Bi2(SO4)3+4
4
NaMnO4+14
14
H2O①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是
Bi2(SO4)3
Bi2(SO4)3
.(1)配平下列离子方程式:______Ix-+______Cl2+______H2O---______Cl-+______I +______,
+______,
在反应中,若消耗Ix-与Cl2物质的量之比为1:8,则x=______.?
(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:Mn2++S2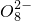 +H2O→Mn
+H2O→Mn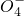 +S
+S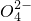 +H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.
+H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.
(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有______.
(4)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
______NaBiO3+______MnSO4+______H2SO4-______Na2SO4+______Bi2(SO4)3+______NaMnO4+______H2O
①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是______.
查看习题详情和答案>>
(1)①配平下列离子方程式:_____I-x+_____Cl2+_____H2O→____Cl-+____IO3-+_______
②在反应中,若消耗I-x与Cl2物质的量之比为1∶8,则x=___________。
(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:
Mn2++S2O82-+H2O→MnO42-+SO42-+H+ 该反应常用于检验Mn2+的存在。其特征现象是__________________________,若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为_______________mol。
(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有_________________。
(4)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:____NaBiO3+____MnSO4+____H2SO4→____Na2SO4+____Bi2(SO4)3+____NaMnO4+____H2O
①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是__________
查看习题详情和答案>>
②在反应中,若消耗I-x与Cl2物质的量之比为1∶8,则x=___________。
(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:
Mn2++S2O82-+H2O→MnO42-+SO42-+H+ 该反应常用于检验Mn2+的存在。其特征现象是__________________________,若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为_______________mol。
(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有_________________。
(4)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:____NaBiO3+____MnSO4+____H2SO4→____Na2SO4+____Bi2(SO4)3+____NaMnO4+____H2O
①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是__________
(1)配平下列离子方程式:______Ix-+______Cl2+______H2O---______Cl-+______I +______,
+______,
在反应中,若消耗Ix-与Cl2物质的量之比为1:8,则x=______.?
(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:Mn2++S2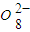 +H2O→Mn
+H2O→Mn +S
+S +H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.
+H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.
(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有______.
(4)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
______NaBiO3+______MnSO4+______H2SO4-______Na2SO4+______Bi2(SO4)3+______NaMnO4+______H2O
①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是______.
查看习题详情和答案>>
 +______,
+______,在反应中,若消耗Ix-与Cl2物质的量之比为1:8,则x=______.?
(2)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发生如下反应:Mn2++S2
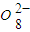 +H2O→Mn
+H2O→Mn +S
+S +H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.
+H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.(3)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有______.
(4)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
______NaBiO3+______MnSO4+______H2SO4-______Na2SO4+______Bi2(SO4)3+______NaMnO4+______H2O
①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是______.
查看习题详情和答案>>