摘要:浓度为0.1mol/L的某物质的水溶液.且PH=5.1.则此物质应是下列中的( ) A.H2SO4 B.NH4Cl C.NaHCO3 D.CH3COONa
网址:http://m.1010jiajiao.com/timu3_id_254803[举报]
亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。
(1)在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I- 被氧化为I2时,产物中含氮的物质为_________(填化学式)。
(2)要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用是_____(填序号)。
a. 稀硫酸 b. 二氧化碳 c. 二氧化硫 d. 磷酸
(3)工业废水中的NO2- 可用铝粉除去。已知此反应体系中包含Al、NaAlO2、NaNO2、
NaOH、NH3、H2O六种物质。将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中:
(1)在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I- 被氧化为I2时,产物中含氮的物质为_________(填化学式)。
(2)要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用是_____(填序号)。
a. 稀硫酸 b. 二氧化碳 c. 二氧化硫 d. 磷酸
(3)工业废水中的NO2- 可用铝粉除去。已知此反应体系中包含Al、NaAlO2、NaNO2、
NaOH、NH3、H2O六种物质。将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中:
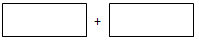
上述反应后废水的pH值将_______(填“上升”、“下降”或“不变”)。
(4)若改用电解法将废水中NO2- 转换为N2除去,N2将在_____(填电极名称)生成
(5)若工业废水中的NO2-的浓度约为1.0×10-4mol/L,取工业废水5mL于试管中,滴加2滴0.1mol/L的硝酸银溶液,能否看到沉淀?(通过计算说明)。(已知Ksp(AgNO2)=2×10-8 mol2·Lˉ2)
查看习题详情和答案>>
(4)若改用电解法将废水中NO2- 转换为N2除去,N2将在_____(填电极名称)生成
(5)若工业废水中的NO2-的浓度约为1.0×10-4mol/L,取工业废水5mL于试管中,滴加2滴0.1mol/L的硝酸银溶液,能否看到沉淀?(通过计算说明)。(已知Ksp(AgNO2)=2×10-8 mol2·Lˉ2)
 (2011?郑州二模)利用所学化学反应原理,解决以下问题:
(2011?郑州二模)利用所学化学反应原理,解决以下问题:(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、N
| H | + 4 |
| H | + 4 |
NH4Cl和NH3?H2O
NH4Cl和NH3?H2O
.(2)0.1mol?L-1的氨水与0.05mol?L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性:
NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
. NH3?H2O+H+
NH3?H2O+H+(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是
R2Z>RX>RY
R2Z>RX>RY
.(4)以石墨电极电解100mL 0.1mol?L-1CuSO4溶液.若阳极上产生气体的物质的量为0.01mol,则阴极上析出Cu的质量为
0.64
0.64
g.(5)向20mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如图所示,B点溶液的pH=7(假设体积可以直接相加),则c(HCl)=
0.2
0.2
mol?L-1.(6)在温度、容积相同的3个密闭容器中,按下表投入反应物,发生反应(H2(g)+
I2(g)?2HI(g)△H=-14.9kJ?mol-1),在恒温、恒容条件下,测得反应达
到平衡时的数据如下表:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol H2、1mol I2 | 2 mol HI | 4 mol HI |
| HI的浓度(mol?L-1) | C1 | C2 | C3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 反应物转化率 | a1 | a2 | a3 |
AC
AC
.A.α1+α2=1 B.2α2=α3 C.a+b=14.9 D.c1=c2=c3.
对一个化学反应的研究需要从反应条件、限度、速率、定量关系等因素进行综合分析,下列是关于化学反应的系列研究,请根据相关信息回答问题.
(1)关于反应物之间的定量关系的研究:已知反应:Br2+2Fe2+═2Br-+2Fe3+,向10mL 0.1mol?L-1的FeBr2溶液中通入0.001mol Cl2,该反应的离子方程式为:
(2)关于反应速率、限度的研究:
①已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,在氯化镁溶液中加入一定量的烧碱,测得pH=13.0,则此温度下残留在溶液中的c(Mg2+)=
②科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气,发生反应:2H2O(g)
2H2(g)+O2(g)△H=+484kJ?mol-1不同时段产生O2的量见下表:
则前20min的反应速率 v(H2O)=

③向某密闭容器中加入 0.3molA、0.1molC和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示.附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,所用条件均不同.已知,t3-t4阶段为使用催化剂[已知t0-t1阶段c(B)未画出].请回答:
I:t4-t5阶段改变的条件为
II:B的起始物质的量为
查看习题详情和答案>>
(1)关于反应物之间的定量关系的研究:已知反应:Br2+2Fe2+═2Br-+2Fe3+,向10mL 0.1mol?L-1的FeBr2溶液中通入0.001mol Cl2,该反应的离子方程式为:
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
(2)关于反应速率、限度的研究:
①已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,在氯化镁溶液中加入一定量的烧碱,测得pH=13.0,则此温度下残留在溶液中的c(Mg2+)=
5.6×10-10mol/L
5.6×10-10mol/L
.②科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气,发生反应:2H2O(g)
| Cu2O |
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
5.0×10-5mol?L-1?min-1
5.0×10-5mol?L-1?min-1
;达平衡时,至少需要吸收的光能为0.968
0.968
kJ.
③向某密闭容器中加入 0.3molA、0.1molC和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示.附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,所用条件均不同.已知,t3-t4阶段为使用催化剂[已知t0-t1阶段c(B)未画出].请回答:
I:t4-t5阶段改变的条件为
减小压强
减小压强
,II:B的起始物质的量为
0.04mol
0.04mol
.对于一个化学反应的研究需要从反应条件、限度、速率、定量关系等因素进行综合分析,下列是关于化学反应的系列研究,请根据相关信息回答问题。
⑴关于反应物之间的定量关系的研究:
已知反 应:Br2 +2Fe2+=2 Br -+2Fe3+,向10 mL0 .1mol/L的Fe Br2溶液中通入0 .003mol Cl2,该反应的离子方程式为
应:Br2 +2Fe2+=2 Br -+2Fe3+,向10 mL0 .1mol/L的Fe Br2溶液中通入0 .003mol Cl2,该反应的离子方程式为
⑵关于反应速率、限度的研究:
①已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,在氯化镁溶液中加入一定量的烧碱,测得pH=13.0,则此温度下残留在溶液中的c(Mg 2+)=
②科学研究发 现纳米级的Cu2O可作为太阳光分解水的催化剂。
现纳米级的Cu2O可作为太阳光分解水的催化剂。
一定温度下 ,在2L密闭容器中加入纳米级的Cu2O并通入0 .1mol水蒸气,发生反应:
,在2L密闭容器中加入纳米级的Cu2O并通入0 .1mol水蒸气,发生反应: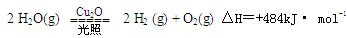 2 H2O(g)
2 H2O(g)
2 H2(g) + O2(g)△H=+484kJ· mol-1,不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
③向某密闭容器中加入0 .3molA、0 .1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示。附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都只改变一种条件。已知t3~t4为使用催化剂,甲图中t0~t1阶段c (B)未画出。请回答:
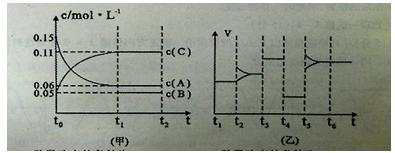
Ⅰ:t4~t5阶段改变的条件是 t5~t6阶段改变的条件是
Ⅱ:B的起始浓度为 ,该反应方程式为 查看习题详情和答案>>