摘要:﹥.﹥.=
网址:http://m.1010jiajiao.com/timu3_id_254678[举报]
|
25℃,下列叙述正确的是 | |
| [ ] | |
A. |
pH=a的醋酸溶液稀释1倍后,溶液的pH=b,则a﹥b |
B. |
0.1 mol/L的碳酸钠溶液的pH小于0.1 mol/L的醋酸钠溶液的pH |
C. |
某物质的溶液pH﹤7,则该物质一定是酸或强酸弱碱盐 |
D. |
0.1 mol/L一元酸HA溶液的pH=3,则NaA溶液存在A-+H2O |
25℃时,下列溶液中微粒的物质的量浓度关系正确的是

A. 的
的 与
与 混合溶液中:
混合溶液中: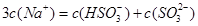
B.0.1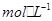 的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)
的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)
C.20mL
0.1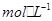 醋酸钠溶液与10mL 0.1
醋酸钠溶液与10mL 0.1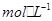 盐酸混合后的溶液中:
盐酸混合后的溶液中:
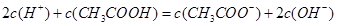
D.在25mL
0.1 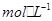
 溶液中逐滴加入0.2
溶液中逐滴加入0.2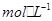
 溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系:
溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系:

查看习题详情和答案>>
25℃时,在20 ml 0.1mol·L-1NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )
|
B.在B点:c(OH-)﹦c(H+),c(Na+)﹦c(CH3COO-)
C.在C点:c(CH3COO-)﹥c(Na+)﹥c(H+) ﹥c(OH-)
D.在C点:c(CH3COO-)+c(CH3COOH)﹦2 c(Na+)
查看习题详情和答案>>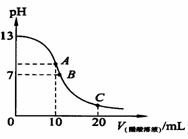

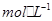 盐酸混合后的溶液中:
盐酸混合后的溶液中: