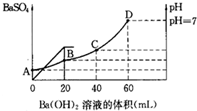
摘要: 往20mL硫酸和盐酸的混合液中.加入0.05mol/L Ba(OH)2溶液时.生成BaSO4的量和溶液的pH变化如右图.计算: (1)最初混合溶液中H2SO4的物质的量浓度, (2)最初混合溶液中HCl的物质的量浓度, (3)B点时溶液的pH是多少?
网址:http://m.1010jiajiao.com/timu3_id_254578[举报]
 往20mL硫酸和盐酸的混合溶液中,加入0.05mol/LBa(OH)2溶液时,生成BaSO4的量和溶液的pH变化如图.试回答:
往20mL硫酸和盐酸的混合溶液中,加入0.05mol/LBa(OH)2溶液时,生成BaSO4的量和溶液的pH变化如图.试回答:(1)起始时,混酸中H2SO4的物质的量浓度为多少?
(2)起始时,混酸中盐酸的物质的量浓度为多少?
(3)B点时溶液的pH是多少?
往20mL硫酸和盐酸的混合溶液中,加入0.05mol/LBa(OH)2溶液时,生成BaSO4的量和溶液的pH变化如右图。试回答: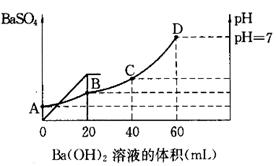
(1)起始时,混酸中H2SO4的物质的量浓度为
(2)起始时,混酸中盐酸的物质的量浓度为
(3)B点时溶液的pH是 。
往20mL硫酸和盐酸的混合溶液中,加入0.05mol/LBa(OH)2溶液时,生成BaSO4的量和溶液的pH变化如右图。试回答:
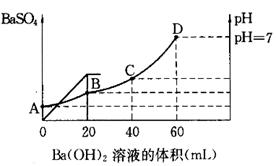
(1)起始时,混酸中H2SO4的物质的量浓度为
(2)起始时,混酸中盐酸的物质的量浓度为
(3)B点时溶液的pH是 。
查看习题详情和答案>>
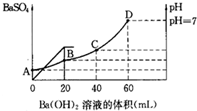 往20mL硫酸和盐酸的混合溶液中,加入0.05mol/L Ba(OH)2溶液时,生成BaSO4的量和溶液的pH变化如图.试回答:
往20mL硫酸和盐酸的混合溶液中,加入0.05mol/L Ba(OH)2溶液时,生成BaSO4的量和溶液的pH变化如图.试回答: