摘要:51.将13.1g镁.铝.铁的混合物与足量的氢氧化钠溶液共热.标准状况下产生3.36L氢气.再将剩余溶液过滤后的残渣跟足量稀H2SO4反应.待完全反应后.标准状况下又产生6.72L氢气.求混合物中各组分的质量分数. 『答案』
网址:http://m.1010jiajiao.com/timu3_id_254479[举报]
(1)将钠、铝、铁各0.3mol分别放入100mL 1mol/L盐酸中,同温同压下产生的气体的体积之比为
(2)将一定量的钠、镁、铝、铁放入足量的稀硫酸中,充分反应中,如果放出的气体在同温同压下体积相同,则消耗的钠、镁、铝、铁的物质的量之比为
(3)将等质量的两份铝单质分别放入足量的稀硫酸和氢氧化钠溶液中,充分反应后,产生的氢气的质量之比为
查看习题详情和答案>>
3:1:1
3:1:1
.(2)将一定量的钠、镁、铝、铁放入足量的稀硫酸中,充分反应中,如果放出的气体在同温同压下体积相同,则消耗的钠、镁、铝、铁的物质的量之比为
6:3:2:3
6:3:2:3
.(3)将等质量的两份铝单质分别放入足量的稀硫酸和氢氧化钠溶液中,充分反应后,产生的氢气的质量之比为
1:1
1:1
,消耗硫酸和氢氧化钠的物质的量之比为3:2
3:2
.将钠、镁、铝、铁四种金属分别跟足量的硫磺反应,消耗硫磺的质量(横坐标)与生成金属硫化物的质量(纵坐标)的关系如图所示(A、B、C、D分别表示一种金属与硫磺反应时的上述质量关系),则这四种金属按A、B、C、D的顺序排列为( )
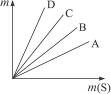
A.Na、Mg、Al、Fe B.Fe、Al、Mg、Na
C.Al、Mg、Na、Fe D.Mg、Al、Na、Fe
查看习题详情和答案>>