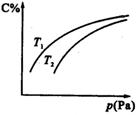
摘要:19.某可逆反应A2C(气).开始均加入1mol A和3mol B.在各种不同温度下.反应经过相同时间.测得C的百分含量c%与温度的关系如图所示: ⑴该正反应是放热反应还是吸热反应 , ⑵T>500℃时c%逐渐减小的原因是 .
网址:http://m.1010jiajiao.com/timu3_id_252602[举报]
一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g)?C(g)+D(g)已达平衡状态的是( )
| A、混合气体的压强不随时间变化而变化 | B、气体总物质的量不随时间变化而变化 | C、2v正(B)=v逆(D) | D、单位时间内消耗n mol C,同时消耗2n mol B |
可逆反应A+3B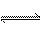
2C +2D,在各种不同的情况下的反应速率分别为:①v(A)=0.15 mol·L-1·s-1,②v(B)=0.6 mol·L-1·s-1,③v(C)=0.4 mol·L-1·s-1,④v(D)=0.45 mol·L-1·s-1。该反应进行最快的是( )
A.① B.②和③ C.④ D.①和④
查看习题详情和答案>>
在密闭容器中,对于可逆反应A+3B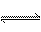
2C (气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是

A.若正反应方向ΔH<0,则T1>T2 B.压强增大时,混合气体的平均相对分子质量减小
C.B一定为气体 D.A一定为气体
查看习题详情和答案>> 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是