摘要: 在 500ml CuSO4和Fe2(SO4)3的混合溶液中加入16.8克铁粉.搅拌并充分反应后.经过滤.洗涤.干燥.可得6.4克铜.要使滤液中SO42-完全沉淀.需加入2.0mol∕L BaCl2溶液500ml.已知Fe3+的氧化性比Cu2+强.求 (1)溶液中SO42-的物质的量浓度 (2)原混合溶液中硫酸铜的物质的量浓度
网址:http://m.1010jiajiao.com/timu3_id_247265[举报]
在500mL CuSO4和Fe2(SO4)3的混合溶液中加入19.6g铁粉,充分反应后,滤出残留固体、洗涤、干燥后称重为16g,在滤液中加入5mol/L BaCl2溶液310mL,恰好使SO42-完全沉淀.求原混合液中CuSO4和Fe2(SO4)3的物质的量浓度.
查看习题详情和答案>>在 400mLCuSO4和Fe2(SO4)3的混合溶液中加入11.2g铁粉,搅拌并充分反应后,经过滤、洗涤、干燥,得到的固体中只含6.4g铜。要使滤液中SO42-完全沉淀,需加入1.0mol/L BaCl2溶液500mL。求:
(1)溶液中SO42-的物质的量浓度。
(2)原混合溶液中CuSO4的物质的量浓度。
查看习题详情和答案>>
(1)溶液中SO42-的物质的量浓度。
(2)原混合溶液中CuSO4的物质的量浓度。
在500mL CuSO4和Fe2(SO4)3的混合液中加入21.7g铁粉,待反应完全后,得到16.8g残留固体.在滤液中加入400mL 4 mol/L的BaCl2溶液,恰好使溶液中的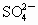 完全沉淀.求:
完全沉淀.求:
(1)残留固体的组成是________.
(2)原混合液中Fe2(SO4)3的浓度为________.
查看习题详情和答案>>