摘要:相同物质的量浓度的两盐溶液NaA溶液和NaB溶液比较.NaA溶液的pH较大.则下列有关同温.同体积.同浓度的HA和HB溶液的叙述中正确的是 A.电离常数:HA>HB B.pH: HA<HB C.与NaOH恰好完全反应时.消耗的NaOH的物质的量:n D.溶液中酸根离子的浓度:C(B-)>C(A-) 20. pH=1的两种酸溶液A.B各1mL.分别加水稀释到1000mL.其pH 与溶液体积的关系如右图所示.下列说法正确的是 A. A.B两种酸溶液的物质的量浓度一定相等 B. 稀释后的A酸溶液的酸性比B酸溶液的酸性强 C. 若a=4,则A是强酸.B是弱酸 D. 若1<a<4.则A.B都是弱酸
网址:http://m.1010jiajiao.com/timu3_id_244856[举报]
下列说法中,能说明酸HA的酸性比酸HB的酸性强的是
A.同温、同浓度的钠盐溶液PH:NaA>NaB
B.PH相同的HA,HB的酸溶液,稀释相同倍数后,PH:HA<HB
C.中和等体积、等PH的HA,HB溶液时,HA消耗NaOH的物质的量多
D.同温、同浓度的两种酸溶液,HA的电离程度大于HB的电离程度
查看习题详情和答案>>
下列说法中,能说明酸HA的酸性比酸HB的酸性强的是
A.同温、同浓度的钠盐溶液PH:NaA>NaB
B.PH相同的HA,HB的酸溶液,稀释相同倍数后,PH:HA<HB
C.中和等体积、等PH的HA,HB溶液时,HA消耗NaOH的物质的量多
D.同温、同浓度的两种酸溶液,HA的电离程度大于HB的电离程度
查看习题详情和答案>>下列图示与对应的叙述相符的是:

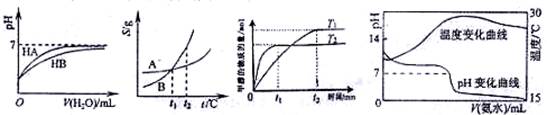
???? ??????? ???? 图1????????????? 图2???????????? 图3???????????????? 图4
A.图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液PH随加水量的变化,则NaA溶液的PH小于同浓度的NaB溶液的PH。
B.图2表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数 B﹥A。
C.图3表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是吸热反应。
D.图4表示将1.000 mol/L氨水滴入20.00mL1.000 mol/L盐酸中,溶液PH和温度随加入氨水体积变化曲线
查看习题详情和答案>>