摘要:30.A.Fe B.Cl2 C.H2 (2)Fe3++3H2O Fe(OH)3+3H+ (3)2Fe3++Fe=3Fe2+
网址:http://m.1010jiajiao.com/timu3_id_243101[举报]
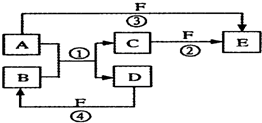 (2010?海南模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的.
(2010?海南模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的.(1)写出B的电子式
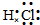
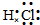
(2)写出反应①的化学方程式
Fe+2HCl=FeCl2+H2↑
Fe+2HCl=FeCl2+H2↑
;(3)E的水溶液显酸性其原因是(用离子方程式表示)
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
;(4)已知3gD和足量F反应放出akJ的热量,请写出表示过程④的热化学方程式
H2(g)+Cl2(g)=2HCl(g)△H=-
kJ/mol
| 2a |
| 3 |
H2(g)+Cl2(g)=2HCl(g)△H=-
kJ/mol
.| 2a |
| 3 |
下列反应的离子方程式书写正确的是
- A.浓烧减溶液中加入铝片:Al+2OH-=AlO2-+H2↑
- B.以石墨作电极电解氯化铝溶液:2Cl-+2H2O
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑ - C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O
- D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3↓+3H+
 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如右(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如右(部分反应中的水已略去).(1)若A为氯碱工业的产品,C为厨房中的用品.
①D的电子式是


②反应Ⅲ的离子方程式是
HCO3-+OH-=H2O+CO32-
HCO3-+OH-=H2O+CO32-
.③氯碱工业制备A的化学方程式是
2NaCl+2H2
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2
2NaOH+H2↑+Cl2↑
,其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1mol KI转移电子0.6mol,则三种物质间反应的离子方程式是
| ||
3Cl2+6OH-+I-=6Cl-+IO3-+3H2O
3Cl2+6OH-+I-=6Cl-+IO3-+3H2O
.(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料.
①反应Ⅲ的离子方程式是
Cl2+2Fe2+=2Cl-+2Fe3+
Cl2+2Fe2+=2Cl-+2Fe3+
.②B可作净水剂,在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是
Fe3++3H2O Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
 Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体Fe3++3H2O Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
. Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体
Fe(OH)3+3H+,酸性条件抑制了Fe3+的水解,不能生成Fe(OH)3胶体