摘要:28. 电化学腐蚀或者吸氧腐蚀. 正极:O2+2H2O+4e-=4OH-,负极:2Fe-4e-=2Fe2+
网址:http://m.1010jiajiao.com/timu3_id_243099[举报]
第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.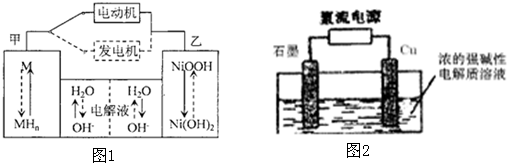
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH
(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
Cu2O+H2阴极的电极反应式是
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
查看习题详情和答案>>

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成lmol水蒸气放热569.1kJ.则该反应的热化学方程式为
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g),△H=-5121.9KJ/mol
| 25 |
| 2 |
C8H18(l)+
O2(g)=8CO2(g)+9H2O(g),△H=-5121.9KJ/mol
.| 25 |
| 2 |
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图1,其总反应式为:H2+2NiOOH
| 放电 |
| 充电 |
增大
增大
(填“增大”、“减小”或“不变”),该电极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-
NiOOH+H2O+e-=Ni(OH)2+OH-
.(3)Cu2O是一种半导体材料,可通过图2的电解装置制取,电解总反应为:2Cu+H2O
| ||
2H++2e-=H2↑
2H++2e-=H2↑
.用镍氢电池作为电源进行电解,当蓄电池中有1mol H2被消耗时,Cu2O的理论产量为144
144
g.(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
吸氧
吸氧
腐蚀.为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的负
负
极(填“正”或“负”)相连.我们知道自然界中的蜘蛛丝和细菌纤维素纤维是典型的纳米纤维。较细的蜘蛛丝直径还不足100纳米,是真正的天然纳米纤维。美国与加拿大的科学家合作,采用蜘蛛基因,利用仿生结构,成功地纺制出人造蜘蛛丝,其强韧性能优于纲材。
(1)纳米纺织材料凭借其内部所特有的小尺寸效应、表面效应等日益受到广大消费者的喜受。许多纳米材料的粒子直径都在1~100nm之间,从分散系的角度看应该属于
。
(2)纳米是长度单位,物质的颗粒达到纳米级时,具有不同的性质,如果单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,下列对“纳米铜”的说法正确的是 (填序号)
A.“纳米铜”与铜片还原性相同
B.“纳米铜”比铜片更易失电子
C.“纳米铜”比铜片的氧化性强
(3)钢铁在人们生活中应用非常广泛,但是钢铁因腐蚀造成的损失全球每年高达7000亿美元,目前钢铁被腐蚀的主要形式是吸氧腐蚀,其正极发生 反应(填“氧化”或“还原”),负极发生的电极反应式为 。为了减少这种腐蚀生产生活中常见的有哪些防腐措施: 。(至少填两种措施)
查看习题详情和答案>>