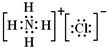摘要:请写出下列物质的电子式 (1)羟基 (2) 乙炔 18在焊接铜漆包线的线头时.常先把线头放在火上烧一下.目的是除去绝缘漆.然后再趁热立即话酒精中蘸一下后再焊接, 请用化学方程式表示其原理 . 19 1.2-二溴乙烷可作汽油抗爆剂.常温下它是无色液体.密度2.18g/cm3.沸点131.4 0C.不溶于水.易溶于醇.醚.丙酮等有机溶剂.在实验室可以用下图所示装置制备1.2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液.试管c中装有液溴(表面覆盖少量水防止挥发). a c d b 填写下列空白 (1) 写出本题中制备1.2-二溴乙烷的两个化学方程式 (2) 容器b中NaOH 溶液的作用是 (3) 某学生做实验时使用了一定量的液溴, 当液溴全部褪色时.所消耗的乙醇和浓硫酸混合液的量比理论值超出许多.如果装置的气密性没有问题.试分析其可能的原因.
网址:http://m.1010jiajiao.com/timu3_id_242634[举报]
已知:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
(1)请写出下列物质的化学式C
(2)分别写出反应④⑥的化学方程式
查看习题详情和答案>>

(1)请写出下列物质的化学式C
NH3
NH3
、乙Al
Al
;(2)分别写出反应④⑥的化学方程式
3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
、2NaOH+2Al+6H2O═2Na[Al(OH)4]+3H2↑
2NaOH+2Al+6H2O═2Na[Al(OH)4]+3H2↑
.
某固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色.
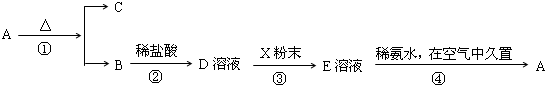
(1)请写出下列物质的化学式:A 、C .
(2)在①②③④各步反应中属于氧化还原反应的有 (填序号).
(3)请分别写出反应①的化学方程式和反应③的离子方程式:① 、③ .
查看习题详情和答案>>

(1)请写出下列物质的化学式:A
(2)在①②③④各步反应中属于氧化还原反应的有
(3)请分别写出反应①的化学方程式和反应③的离子方程式:①
已知A、B、C、D、E、F 六种物质的转化关系如下:
①A+B→C+H2O
②C+KOH→D↓(蓝色)+E
③B+D→C+H2O
④E+BaCl2→KCl+F↓(白色,不溶于稀硝酸)
⑤G+B→CO2↑+F↓+H2O,反应中B与CO2的物质的量之比为1:2
根据上述变化关系填空:
(1)请写出下列物质的化学式:B
(2)检验E中阴离子的实验方法是
(3)往G的溶液中滴加过量的KOH,反应的离子方程式为
查看习题详情和答案>>
①A+B→C+H2O
②C+KOH→D↓(蓝色)+E
③B+D→C+H2O
④E+BaCl2→KCl+F↓(白色,不溶于稀硝酸)
⑤G+B→CO2↑+F↓+H2O,反应中B与CO2的物质的量之比为1:2
根据上述变化关系填空:
(1)请写出下列物质的化学式:B
H2SO4
H2SO4
;CCuSO4
CuSO4
;GBa(HCO3)2
Ba(HCO3)2
.(2)检验E中阴离子的实验方法是
先加入足量的稀盐酸,再加入氯化钡溶液,若有白色沉淀生成,则含有SO42-
先加入足量的稀盐酸,再加入氯化钡溶液,若有白色沉淀生成,则含有SO42-
(3)往G的溶液中滴加过量的KOH,反应的离子方程式为
Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O
Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O
.