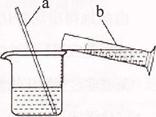
摘要:配制l00g溶质质量分数为6%的氢氧化钠溶液(水的密度近似看作l g/cm3).下列操作正确的是( ) A.将氢氧化钠固体置于滤纸上 B.俯视量筒刻度读出所取水的体积 C.将氢氧化钠固体置于托盘天平的右盘.砝码置于左盘称量 D.将94 mL水倒入盛有6g氢氧化钠的烧杯中搅拌溶解
网址:http://m.1010jiajiao.com/timu3_id_24234[举报]
 (2012?牡丹江)实验室用98%的浓硫酸(密度为1.84g/ml)配制l00g溶质质量分数为20%的稀硫酸.
(2012?牡丹江)实验室用98%的浓硫酸(密度为1.84g/ml)配制l00g溶质质量分数为20%的稀硫酸.(1)配制该溶液的步骤:
计算
计算
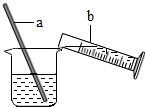
、量取、溶解、装瓶贴标签;(2)溶解过程如图所示,b中盛放的物质是
浓硫酸
浓硫酸
,a的作用是搅拌,使热量尽快散失(合理说法均可)
搅拌,使热量尽快散失(合理说法均可)
;(3)实验过程中如果不慎将浓硫酸沾到皮肤上应立即
大量水冲洗
大量水冲洗
,然后涂上3%-5%的碳酸氢钠溶液;(4)配制后溶液中溶质的质量分数小于20%,分析引起这一结果的原因可能是
用量筒量取水时仰视读数(合理均可)
用量筒量取水时仰视读数(合理均可)
(写出一种即可).实验室用98%的浓硫酸(密度为1.84g/ml)配制l00g溶质质量分数为20%的稀硫酸。
(1)配制该溶液的步骤: 、量取、溶解、装瓶贴标签;
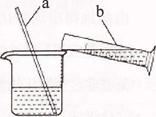
(2)溶解过程如右图所示,b中盛放的物质是 ,a的作用是 ;
(3)实验过程中如果不慎将浓硫酸沾到皮肤上应立即 , 然后涂上3%—5%的碳酸氢钠溶液;
(4)配制后溶液中溶质的质量分数小于20%,分析引起这一结果的原因可能是 (写出一种即可)。