摘要:某化学反应 2A B + D 在四个不同条件下进行.B.D起始为0.反应物A的浓度变化情况如下表: 实验序号 0 10 20 30 40 50 60 1 800℃ 1.0 0.8 0.67 0.57 0.50 0.50 0.50 2 800℃ C2 0.60 0.50 0.50 0.50 0.50 0.50 3 800℃ C3 0.92 0.75 0.63 0.60 0.60 0.60 4 820℃ 1.0 0.40 0.25 0.20 0.20 0.20 0.20 根据表中数据完成下列填空: (1)在实验1.反应在10至20min内的平均速率为 mol/ (2)在实验2,A的初始浓度C2= mol/L.反应经20 min就达到平衡,可推测实验2中还隐含的条件是 . (3)设实验3的反应速率为υ3,实验1的反应速率为υ1,则υ3 υ1 (填"<","=",">").且C3 1.0 mol/L (填"<",">"或"="). (4)比较实验4和实验1,可推测该反应 反应.理由是: .
网址:http://m.1010jiajiao.com/timu3_id_238095[举报]
某化学反应2A(g)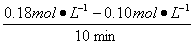 B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物B的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物B的浓度(mol/L)随反应时间(min)的变化情况如下表:
序号 | 浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
① | 0 | 0.10 | 0.18 | 0.22 | 0.25 | 0.25 | 0.25 | |
② | 0 | 0.20 | C2 | C2 | C2 | C2 | C2 | |
③ | 0 | 0.040 | 0.22 | 0.24 | 0.30 | 0.30 | 0.30 | |
④ | 0 | 0.30 | 0.37 | 0.40 | 0.40 | 0.40 | 0.40 |
根据上述数据,完成下列填空:
(1)在①中,A的起始浓度为1 mol/L,反应在10至20 min内,A的平均速率为______________mol/L·min。
(2)在②中,A的起始浓度为1 mol/L,则C2=______mol/L。由实验数据可知,与①相比,在②中多了一个条件__________________。
(3)观察③的数据,判断A的起始浓度__________________1 mol/L(填“>”“=”“<”)。
(4)已知④中A的起始浓度为1 mol/L,通过比较__________________(填实验序号)的实验数据,可推测该反应ΔH__________________0(填“>”或“<”)。
查看习题详情和答案>>