摘要:在一定条件下.Cl2与NH4Cl发生反应:xCl2+yNH4Cl=yNClx+(x+y)HCl.已知当消耗6.72L Cl2时.生成0.1mol氮的氯化物.则该氯化物的化学式为 ( ) A.NCl2 B.NCl3 C.NCl4 D.NCl5 答案:B[提示:当消耗0.3mol Cl2时生成0.1mol氮的氯化物.由阿伏加德罗定律可知.有反应关系:3Cl2+yNH4Cl=NClx+(x+y)HCl,由N元素守恒可知y=1,由H元素守恒可知x=3.故B项正确]
网址:http://m.1010jiajiao.com/timu3_id_238048[举报]
在一定条件下,Cl2与NH4Cl可发生如下反应:xCl2+YNH4Cl=NClx+(x+y)HCl,已知当消耗6.72升 Cl2(标准状况)时,生成0.1 mol氮的氯化物,则它的化学式为( )?
A.NCl2 B.NCl3 C.NCl4 D.NCl5?
查看习题详情和答案>>
在一定条件下,Cl2与NH4Cl可发生如下反应: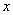 Cl2+
Cl2+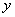 NH4Cl
NH4Cl NClx+(
NClx+(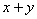 )HCl,已知当消耗6.72升Cl2(标准状况)时,生成0.1 mol氮的氯化物,则它的化学式为?( )
)HCl,已知当消耗6.72升Cl2(标准状况)时,生成0.1 mol氮的氯化物,则它的化学式为?( )
A.NCl2 B.NCl3?
C.NCl4 D.NCl5??
查看习题详情和答案>>在一定条件下,Cl2与NH4Cl可发生如下反应:xCl2+yNH4Cl=yNClx+(x+y)HCl.已知当消耗6.72L Cl2时(标准状况),生成0.1mol氮的氯化物,则该氯化物的化学式为
- A.NCl2
- B.NCl3
- C.NCl4
- D.NCl5
在一定条件下,Cl2与NH4Cl可发生如下反应:xCl2+yNH4Cl→yNClx+(x+y)HCl则该氮的氯化物的化学式为:
A、NCl2 B、NCl3 C、NCl4 D、NCl5
查看习题详情和答案>>|
在一定条件下,Cl2与NH4Cl可发生如下反应:xCl2=yNH4Cl | |
| [ ] | |
A. |
NCl2 |
B. |
NCl3 |
C. |
NCl4 |
D. |
NCl5 |