摘要:把除去氧化膜的镁条投入到盛有少量稀盐酸的试管中.发现氢气发生的速率变化情况如图所示.其中t1-t2速率变化的主要原因是 ,t2-t3速率变化的主要原因是 . 解析:Mg与HCl溶液的反应是放热反应.该反应中并存两个影响化学反应速率的外因:一是反应放出的热能使反应体系温度升高.化学反应速率增大,二是反应使HCl物质的量浓度减小.化学反应速率减小.由图像可知.在t1-t2的时间内温度变化是影响化学反应速率的主要外因.在t2-t3的时间内.HCl物质的量浓度的变化是影响化学反应速率的主要外因. 答案:反应是放热反应.温度升高使化学反应速率提高 HCl物质的量浓度变小使化学反应速率降低 10分钟训练(强化类训练.可用于课中)
网址:http://m.1010jiajiao.com/timu3_id_235526[举报]
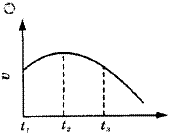
把除去氧化膜的镁条投入到盛有少量稀盐酸的试管中,发现氢气发生的速率变化情况如下图所示。其中t1~t2速率变化的主要原因是_____________________;t2~t3速率变化的主要原因是 。?

把除去氧化膜的镁条投入到盛有少量稀盐酸的试管中,发现氢气发生的速率变化情况如图所示。其中t1—t2速率变化的主要原因是________________________________________;t2—t3速率变化的主要原因是________________________________________。

把除去氧化膜的镁条投入到盛有少量稀盐酸的试管中,发现氢气发生的速率变化情况如图所示。

其中t1—t2速率变化的主要原因是______________;t2—t3速率变化的主要原因是______________。
查看习题详情和答案>>