摘要:25.实验室制取氯气除了用浓盐酸和二氧化锰反应外还可运用下列反应:KClO3 + 6HCl = KCl + 3Cl2↑ + 3H2O.该反应的优点是反应产生氯气速度快.不需加热. (1)上述反应中 是还原剂. 元素被还原.若反应产生
网址:http://m.1010jiajiao.com/timu3_id_227546[举报]
实验室制取氯气除了用浓盐酸和二氧化锰反应外还可运用下列反应:KClO3+6HCl=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热.________(1)上述反应中________是还原剂,________元素被还原,若反应产生0.3 mol氯气,则转移的电子数目为________.
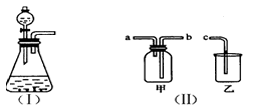
下图(Ⅰ)是实验室制取气体的一种发生装置.

(1)若用上述装置制取O2,除了可选择二氧化锰和________(物质名称)反应外,还能选择一种物质和水反应,写出后一个反应的化学方程式________.
(2)用排空气法收集H2,可选择图(Ⅱ)中的甲装置,收集时气体应从________口进气.(填“a”或“b”)
(3)实验室以KMnO4和浓盐酸为反应物,利用(Ⅰ)、(Ⅱ)装置组合制取氯气,反应方程式如下:
________KMnO4+________HCl=________KCl+________MnCl2+________Cl2↑+________H2O①配平上述反应方程式(在空格里填上适合的计量系数),并标出电子转移的方向和数目.
②组合装置乙中盛放氢氧化钠溶液,其作用为________,发生反应的离子方程式为________.
下图(I)是实验室制取气体的一种发生装置。
(1)若用上述装置制取O2,除了可选择二氧化锰和_________(物质名称)反应外, 还能选择一种物质和水反应,写出后一个反应的化学方程式____。
(2)用排空气法收集H2,可选择图(Ⅱ)中的甲装置,收集时气体应从____口 进气(填“a”或“b”)。
(3)实验室以KMnO4和浓盐酸为反应物,利用(I)、(Ⅱ)装置组合制取氯气,反应方程式如下:
___ KMnO4+____HCl=____KCl+____MnCl2+____Cl2+____H2O
①配平上述反应方程式(在空格里填上适合的计量系数),并标出电子转移的方 向和数目。
②组合装置乙中盛放氢氧化钠溶液,其作用为____, 发生反应的离子方程式为________。
查看习题详情和答案>>
(2)用排空气法收集H2,可选择图(Ⅱ)中的甲装置,收集时气体应从____口 进气(填“a”或“b”)。
(3)实验室以KMnO4和浓盐酸为反应物,利用(I)、(Ⅱ)装置组合制取氯气,反应方程式如下:
___ KMnO4+____HCl=____KCl+____MnCl2+____Cl2+____H2O
①配平上述反应方程式(在空格里填上适合的计量系数),并标出电子转移的方 向和数目。
②组合装置乙中盛放氢氧化钠溶液,其作用为____, 发生反应的离子方程式为________。
(2011?中山三模)实验室用浓盐酸和二氧化锰制备氯气并用所制氯气制备少量氯水的装置图如下,回答有关问题.
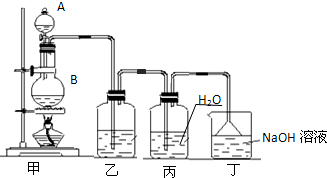
(1)从仪器A向仪器B中加入浓盐酸的操作方法是
(2)装置乙中盛放的试剂是
(3)写出氯气与水反应的化学方程式
(4)某同学设计了一个实验方案以证明新制氯水中含有次氯酸.他所用的试剂如下:
新制氯水 0.5mol.L-1CaCl2溶液 品红溶液 CaCO3粉末
请你协助完成实验方案.
步骤一:取5mL0.5mol.L-1CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色.
步骤二:取5mL新制氯水于试管中,
步骤三:
说明新制氯水中存在次氯酸的实验现象是
(5)设计步骤一的理由是
查看习题详情和答案>>

(1)从仪器A向仪器B中加入浓盐酸的操作方法是
取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体
取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体
.反应中控制氯气产生速率大小的方法是通过控制浓盐酸的加入速度来控制氯气的产生速率
通过控制浓盐酸的加入速度来控制氯气的产生速率
.(2)装置乙中盛放的试剂是
饱和食盐水
饱和食盐水
,其作用是除去氯气中的氯化氢
除去氯气中的氯化氢
.(3)写出氯气与水反应的化学方程式
Cl2+H2O=HCl+HClO
Cl2+H2O=HCl+HClO
.(4)某同学设计了一个实验方案以证明新制氯水中含有次氯酸.他所用的试剂如下:
新制氯水 0.5mol.L-1CaCl2溶液 品红溶液 CaCO3粉末
请你协助完成实验方案.
步骤一:取5mL0.5mol.L-1CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色.
步骤二:取5mL新制氯水于试管中,
加入碳酸钙粉末充分反应至溶液无色
加入碳酸钙粉末充分反应至溶液无色
.步骤三:
取上层清液于另一试管中加入3滴品红溶液,振荡
取上层清液于另一试管中加入3滴品红溶液,振荡
.说明新制氯水中存在次氯酸的实验现象是
品红溶液褪色
品红溶液褪色
.(5)设计步骤一的理由是
氯水与碳酸钙反应后生成氯化钙溶液,为证明品红溶液褪色是次氯酸的作用,须实验证明氯化钙溶液不具漂白性(或“排除氯化钙溶液的干扰”)
氯水与碳酸钙反应后生成氯化钙溶液,为证明品红溶液褪色是次氯酸的作用,须实验证明氯化钙溶液不具漂白性(或“排除氯化钙溶液的干扰”)
.氯气是一种重要的化工原料.某学习小组在实验室中利用如图所示装置制取氯气并探究其性质.
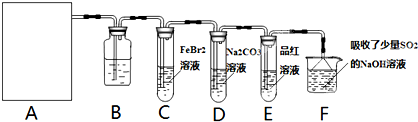
(1)若A是用二氧化锰和浓盐酸反应制取氯气的发生装置,除圆底烧瓶和导管外还用到的玻璃仪器有
(2)①装置B中盛有的试剂是
②若E中品红溶液褪色,则C装置中发生反应的离子方程式是
③已知碳酸的酸性强于次氯酸,则装置D中反应的化学方程式为
(3)某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解;在碱性条件下ClO-也有强氧化性.).
①提出合理假设:
假设1:只存在SO32-;
假设2:只存在ClO-;
假设3:既存在SO32-,也存在ClO-;
假设4:既不存在SO32-,也不存在ClO-.
指导老师经分析认为,其中一个假设并不合理,它是
②设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.限选实验试剂.
a.3mol/L H2SO4 b.0.01mol/L KMnO4 c.1mol/L BaCl2溶液
d.淀粉一KI溶液 e.酚酞试液 f.品红溶液
步骤一;取少量吸收液于试管中,滴加3mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加1~2滴
步骤三:向B试管中滴加1~2滴
③若假设2成立;写出步骤三中的离子方程式:
查看习题详情和答案>>

(1)若A是用二氧化锰和浓盐酸反应制取氯气的发生装置,除圆底烧瓶和导管外还用到的玻璃仪器有
分液漏斗、酒精灯
分液漏斗、酒精灯
;(2)①装置B中盛有的试剂是
饱和食盐水
饱和食盐水
,作用是除去氯气中的氯化氢杂质
除去氯气中的氯化氢杂质
.②若E中品红溶液褪色,则C装置中发生反应的离子方程式是
2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2
2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2
.证明FeBr2与Cl2发生了氧化还原反应的实验方法是实验后取下装置C的橡胶塞,取少量C中溶液于试管中,滴加KSCN溶液
实验后取下装置C的橡胶塞,取少量C中溶液于试管中,滴加KSCN溶液
(填操作方法).③已知碳酸的酸性强于次氯酸,则装置D中反应的化学方程式为
2Cl2+Na2CO3 +H2O=CO2+2NaCl+2HClO
2Cl2+Na2CO3 +H2O=CO2+2NaCl+2HClO
.(3)某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解;在碱性条件下ClO-也有强氧化性.).
①提出合理假设:
假设1:只存在SO32-;
假设2:只存在ClO-;
假设3:既存在SO32-,也存在ClO-;
假设4:既不存在SO32-,也不存在ClO-.
指导老师经分析认为,其中一个假设并不合理,它是
假设3
假设3
;判断的原因是ClO-与SO32-因发生氧化还原反应而不能大量共存
ClO-与SO32-因发生氧化还原反应而不能大量共存
.②设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.限选实验试剂.
a.3mol/L H2SO4 b.0.01mol/L KMnO4 c.1mol/L BaCl2溶液
d.淀粉一KI溶液 e.酚酞试液 f.品红溶液
步骤一;取少量吸收液于试管中,滴加3mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加1~2滴
b
b
(填序号).若溶液褪色
褪色
(填现象),则假设1成立.步骤三:向B试管中滴加1~2滴
d
d
(填序号);若溶液变蓝色
变蓝色
(填现象),则假设2成立.③若假设2成立;写出步骤三中的离子方程式:
2I-+ClO-+2H+═I2+H2O+Cl-
2I-+ClO-+2H+═I2+H2O+Cl-
.