摘要:0.4 g 1.204×1023
网址:http://m.1010jiajiao.com/timu3_id_225846[举报]
下列叙述正确的是
- A.标准状况下的气体摩尔体积约为22.4 L
- B.H2的摩尔质量为2 g/mol
- C.摩尔是用来衡量微观粒子多少的一种物理量
- D.0.1 molH2SO4含有氢原子数的准确值为1.204×1023
|
下列叙述正确的是 | |
| [ ] | |
A. |
标准状况下的气体摩尔体积约为22.4 L |
B. |
H2的摩尔质量为2 g/mol |
C. |
摩尔是用来衡量微观粒子多少的一种物理量 |
D. |
0.1 mol H2SO4含有氢原子数的准确值为1.204×1023 |
 A、B、C、D、E五种短周期元素,原子序数依次递增.A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,E与C是同主族元素.C、D两种元素可形成化合物甲,甲中既有离子键又有共价键;A、B、C、D四种元素可形成化合物乙,乙放入水中所得溶液显碱性.请回答:
A、B、C、D、E五种短周期元素,原子序数依次递增.A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,E与C是同主族元素.C、D两种元素可形成化合物甲,甲中既有离子键又有共价键;A、B、C、D四种元素可形成化合物乙,乙放入水中所得溶液显碱性.请回答:(1)化合物甲的电子式为
Na+[ ]2-Na+
]2-Na+
 ]2-Na+
]2-Na+Na+[ ]2-Na+
]2-Na+
;乙的化学式有很多种,其中无机物是 ]2-Na+
]2-Na+NaHCO3
NaHCO3
,相对分子质量最小的有机物是CH3ONa
CH3ONa
.(2)气体A2、C2和A、C、D形成的离子化合物的水溶液可形成燃料电池,其正极的电极反应式为
O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
,电池总反应得到1.8g产物时,流经外电路某一横截面的电子数为1.204×1023(或0.2NA)
1.204×1023(或0.2NA)
.(3)A、B能形成无数种化合物,其中密度最小的气态化合物燃烧热为890.3 kJ/mol,该化合物燃烧的热化学方程式为
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ?mol-1
.(4)都由A、C、D、E形成的两种化合物可以相互反应,其离子方程式为
H++HSO3-═SO2↑+H2O
H++HSO3-═SO2↑+H2O
. (2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.
(2013?绵阳模拟)A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大.其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的 简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体.(1)M的基态原子价层电子排布式为
3d24s2
3d24s2
,元素B、D、G的第一电离能由大到时小的顺序是N>O>S
N>O>S
(用元素符号表示).(2)用价层电子对互斥理论预测,GD32-的立体构型是
三角锥型
三角锥型
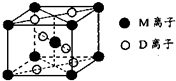
(用文字表述)(3)M与D形成的一种橙红色晶体晶胞结构如图所示,其化学式为
TiO2
TiO2
(用元素符号表示).(4)已知化合物EB结构与单晶硅相似,该物质可由E 的氯化物与NaB3在高温下反应制得,且生成单质B2,该反应化学方程式为
AlCl3+3NaN3═3NaCl+AlN+4N2↑
AlCl3+3NaN3═3NaCl+AlN+4N2↑
,若有8.4gB2生成,则转移电子数为1.204×1023或0.2NA
1.204×1023或0.2NA
.