摘要:21.归纳总结是学习化学的重要方法.小明同学用图l总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应). (l)为了验证反应①.小明将无色酚嗽试液滴入NaOH液中.溶液变成 红 色. (2)依据反应②说明NaOH必须密封保存.否则在空气中要变质.其化学反应方程式为:2NaOH + CO2 === Na2 CO3 + H2 O. (3)小明用徽观示意图(图2)来说明反应③的发生.用化学反 应方程式表示为: 2NaOH + H2SO4 === Na2SO4+2H2 O.. 从该图可以看出.反应前后没有发生变化的徽观粒子有Na+-和SO42-. (4)为了验证反应④能够发生.你选择的物质是 C . A.Na2CO3 B.HCl C.CuSO4 D.NaCl
网址:http://m.1010jiajiao.com/timu3_id_22539[举报]
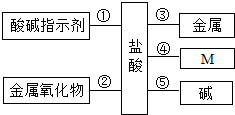 归纳总结是学习化学的重要方法,小莉同学用如图总结了盐酸与其它物质反应的①~⑤五条化学性质.
归纳总结是学习化学的重要方法,小莉同学用如图总结了盐酸与其它物质反应的①~⑤五条化学性质.(1)铁生锈是铁与
氧气和水
氧气和水
发生反应,盐酸可除去铁表面的铁锈是利用盐酸在如图的性质②
②
.(填序号)(2)下列物质可以利用盐酸的性质③制得的是
D
D
(填序号):A、CuCl2 B、AgCl C、FeCl3 D、ZnCl2
(3)盐酸溶液与硫化亚铁固体能发生复分解反应,该反应的化学方程式为:
2HCl+FeS=H2S↑+FeCl2
2HCl+FeS=H2S↑+FeCl2
.(4)归纳盐酸性质④的化学反应规律:
盐酸能与盐反应生成新酸和新盐
盐酸能与盐反应生成新酸和新盐
.11、归纳总结是学习化学的有效方法.以下是某同学关于实验方面的一些归纳总结,请你一起完成:
(1)实验室中有些药品需密封保存的原因:
A.药品能吸收空气中的水蒸气;B.药品能与空气中的某些成分发生化学反应;C.药品易挥发;D.药品具有腐蚀性.
氢氧化钠固体需要密封保存,其原因是(填编号)
(2)影响化学反应速率的因素有催化剂、温度、反应物浓度、反应物的接触面积等.请你举一例说明 :反应物的浓度越大,反应速率越大.
:反应物的浓度越大,反应速率越大.
(3)已知20℃硫酸铜的溶解度为20g,水的密度大约为1g/cm3.20℃时,在三支试管中各加入10mL水,然后分别加入约0.5g、1.5g、2.5g无水硫酸铜,如图所示.
充分震荡.然后仔细观察现象,发现有③号试管中的现象与①、②号试管明显不同,其现象是
查看习题详情和答案>>
(1)实验室中有些药品需密封保存的原因:
A.药品能吸收空气中的水蒸气;B.药品能与空气中的某些成分发生化学反应;C.药品易挥发;D.药品具有腐蚀性.
氢氧化钠固体需要密封保存,其原因是(填编号)
A B
,涉及的化学方程式为2NaOH+CO2=Na2CO3+H2O
.(2)影响化学反应速率的因素有催化剂、温度、反应物浓度、反应物的接触面积等.请你举一例说明
 :反应物的浓度越大,反应速率越大.
:反应物的浓度越大,反应速率越大.硫在氧气中燃烧
.(3)已知20℃硫酸铜的溶解度为20g,水的密度大约为1g/cm3.20℃时,在三支试管中各加入10mL水,然后分别加入约0.5g、1.5g、2.5g无水硫酸铜,如图所示.
充分震荡.然后仔细观察现象,发现有③号试管中的现象与①、②号试管明显不同,其现象是
有蓝色晶体出现
.若要使②号试管里的溶液转化成③号试管里的溶液,最简单的方法是加入硫酸铜固体
.(2010?韶关)归纳总结是学习化学的有效方法.小明同学在做实验的过程中,发现一瓶氢氧化钠溶液因为没有密封保存而变质了,于是他将药品需密封保存的原因进行了归纳总结,请你帮助他一起完成:
(1)你认为氢氧化钠溶液变质的原因是
(2)除以上情况外,你认为有些药品需密封保存的原因还有:
①
②
查看习题详情和答案>>
(1)你认为氢氧化钠溶液变质的原因是
CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
(用化学方程式表示),由此你可以总结出有些药品需密封保存的原因是:药品能与空气中的某些成分发生化学反应
药品能与空气中的某些成分发生化学反应
.(2)除以上情况外,你认为有些药品需密封保存的原因还有:
①
药品能吸收空气中的水蒸气;
药品能吸收空气中的水蒸气;
;写出一个符合情况①的药品名称浓硫酸
浓硫酸
②
药品易挥发
药品易挥发
.写出一个符合情况②的药品名称浓盐酸
浓盐酸
.