摘要:27. Cu+2H2SO4(浓)CuSO4 + SO2↑+2H2OK^S*5U.C#O% (2) 蘸有品红溶液的滤纸褪色¥高#考#资%源* (3)吸收多余的SO2.防止污染空气. A B
网址:http://m.1010jiajiao.com/timu3_id_217146[举报]
工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:CuO+2HCl═CuCl2+H2O FeO+2HCl═FeCl2+H2O; 已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.除去溶液中的Fe2+,可以采用的方法是( )
查看习题详情和答案>>
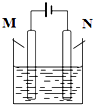 如图所示,用石墨作电极电解氯化铜溶液,下列说法正确的是( )
如图所示,用石墨作电极电解氯化铜溶液,下列说法正确的是( )