摘要:下表列出了A~R几种元素在周期表中的位置 周期 族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 2 E F 3 A C D I G R 4 B H (1)画出R原子结构示意图 . (2)上述元素的最高价氧化物对应的水化物中.其碱性最强的是 .酸性最强的是 . (3)上述元素的气态氢化物中.E元素的氢化物的结构式为 .F元素组成单质的电子式为 . (4)用电子式表示C元素和H元素形成的化合物的形成过程 . (5)写出D的最高价氧化物与B的最高价氧化物对应的水化物反应的离子反应方程式 . (6)写出单质E与I的最高价氧化物对应的水化物浓溶液反应的化学方程式 (7)可以验证C.D两元素金属性强弱的实验是 . (a)将在空气中放置已久的这两种元素的块状单质分别放入热水中 (b)将形状.大小相同的这两种元素的单质分别和同浓度的盐酸反应 (c)将形状.大小相同这两种元素的单质分别和热水作用.并滴入酚酞溶液 (d)比较这两种元素的气态氢化物的稳定性
网址:http://m.1010jiajiao.com/timu3_id_214741[举报]
(10分).
Ⅰ. 下表列出了A~R 9种元素在周期表中的位置(填元素符号):
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | E | | F | | |
| 3 | A | C | D | | | | G | R |
| 4 | B | | | | | | H | |
(2) A、B、C三种元素按原子半径由大到小的顺序排列为
(3) F元素氢化物的化学式是
(4) G元素跟B元素形成化合物的电子式是
(5) G元素和H元素两者核电荷数之差是
Ⅱ 根据原子结构的有关知识和元素周期律。思考并回答有关114号元素的几个问题。
原子核外有_____个电子层,最外层电子数可能是__________
周期表中位于__________周期,________族
(3) 属于_________元素(填金属或非金属) 查看习题详情和答案>>
(10分).
Ⅰ. 下表列出了A~R 9种元素在周期表中的位置(填元素符号):
(1) 这9种元素中化学性质最不活泼的是__________,
(2) A、B、C三种元素按原子半径由大到小的顺序排列为
(3) F元素氢化物的化学式是
(4) G元素跟B元素形成化合物的电子式是
(5) G元素和H元素两者核电荷数之差是
Ⅱ 根据原子结构的有关知识和元素周期律。思考并回答有关114号元素的几个问题。
原子核外有_____个电子层,最外层电子数可能是__________
周期表中位于__________周期,________族
(3) 属于_________元素(填金属或非金属)
Ⅰ. 下表列出了A~R 9种元素在周期表中的位置(填元素符号):
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | E | | F | | |
| 3 | A | C | D | | | | G | R |
| 4 | B | | | | | | H | |
(2) A、B、C三种元素按原子半径由大到小的顺序排列为
(3) F元素氢化物的化学式是
(4) G元素跟B元素形成化合物的电子式是
(5) G元素和H元素两者核电荷数之差是
Ⅱ 根据原子结构的有关知识和元素周期律。思考并回答有关114号元素的几个问题。
原子核外有_____个电子层,最外层电子数可能是__________
周期表中位于__________周期,________族
(3) 属于_________元素(填金属或非金属)
下表列出了九种元素在元素周期表中的位置:
根据题意,用元素符号或化学式填空:
(1)这几种元素中,金属性最强的是
(2)G元素和H元素的核电荷数之差是
(3)A、B、C三种元素的原子半径由大到小的顺序为
(4)用电子式表示H元素跟A元素形成化合物的过程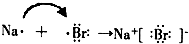
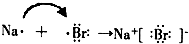 .
.
(5)C、D两元素比较,金属性较强的是
①将在空气中放置已久的C和D的单质分别与热水反应
②将除去氧化物薄膜的C与D的单质分别和热水作用,并滴入酚酞溶液
③将除去氧化物薄膜的C与D的单质分别和2mL1mol?L-1的盐酸反应
④比较这两种元素的气态氢化物的稳定性
(6)D和F两种元素形成的化合物与强碱反应的离子方程式为
查看习题详情和答案>>
族 周期 |
I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)这几种元素中,金属性最强的是
K
K
;化学性质最不活泼的是Ar
Ar
.(2)G元素和H元素的核电荷数之差是
18
18
;含有6个中子的E原子的化学符号为126C
126C
.(3)A、B、C三种元素的原子半径由大到小的顺序为
K>Na>Mg
K>Na>Mg
.(4)用电子式表示H元素跟A元素形成化合物的过程
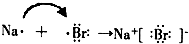
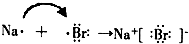
(5)C、D两元素比较,金属性较强的是
Mg
Mg
,可以验证该结论的实验是②③
②③
(用编号表示).①将在空气中放置已久的C和D的单质分别与热水反应
②将除去氧化物薄膜的C与D的单质分别和热水作用,并滴入酚酞溶液
③将除去氧化物薄膜的C与D的单质分别和2mL1mol?L-1的盐酸反应
④比较这两种元素的气态氢化物的稳定性
(6)D和F两种元素形成的化合物与强碱反应的离子方程式为
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.