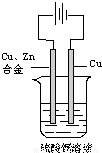
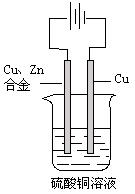
摘要:如图:以一铜锌合金为阳极.一纯铜为阴极. 进行电解.电解液为硫酸铜溶液.当外电路有1.806×1023个电子转移时. 阴极比阳极重19.25g .求铜锌合金中铜的质量分数. (已知:电极反应式为 阳极: Zn-2e-=Zn2+.Cu-2e-=Cu2+ 阴极:Cu2+ +2e-=Cu ) 2009-20010学年度第二学期期中考试
网址:http://m.1010jiajiao.com/timu3_id_213631[举报]
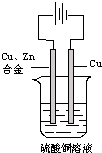 如图:以一铜锌合金为阳极,一纯铜为阴极(起始时两电极质量相等),进行电解,电解液为硫酸铜溶液,当外电路有1.806×1023个电子转移时,阴极比阳极重19.25g,求铜锌合金中铜的质量分数.
如图:以一铜锌合金为阳极,一纯铜为阴极(起始时两电极质量相等),进行电解,电解液为硫酸铜溶液,当外电路有1.806×1023个电子转移时,阴极比阳极重19.25g,求铜锌合金中铜的质量分数.(已知:电极反应式为 阳极:Zn-2e-=Zn2+、Cu-2e-=Cu2+阴极:Cu2++2e-=Cu )
(3分)如图:以一铜锌合金为阳极,一纯铜为阴极(起始时两电极质量相等),进行电解,电解液为硫酸铜溶液,当外电路有1.806×1023个电子转移时,阴极比阳极重19.25g ,求铜锌合金中铜的质量分数。

(已知:电极反应式为 阳极: Zn-2e-=Zn2+、Cu-2e-=Cu2+
阴极:Cu2+ +2e-=Cu )
查看习题详情和答案>>
如图:以一铜锌合金为阳极,一纯铜为阴极(起始时两电极质量相等),进行电解,电解液为硫酸铜溶液,当外电路有1.806×1023个电子转移时,阴极比阳极重19.25g,求铜锌合金中铜的质量分数.
(已知:电极反应式为 阳极:Zn-2e-=Zn2+、Cu-2e-=Cu2+阴极:Cu2++2e-=Cu )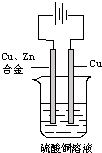
查看习题详情和答案>>
(已知:电极反应式为 阳极:Zn-2e-=Zn2+、Cu-2e-=Cu2+阴极:Cu2++2e-=Cu )