摘要:下列说法中正确的是 A.常温常压下.1 mol H2的体积约为22.4 L B.标准状况下.11.2 L氢气中含约含3.01×1023个氢原子 C.在标准状况下.1 mol H2O所占体积约为22.4 L D.在同温同压下.相同体积的任何气体所含的分子数相同
网址:http://m.1010jiajiao.com/timu3_id_213001[举报]
|
下列说法中正确的是 | |
A. |
标准状况下, 1 mol CH4和丙烷(气体)的混合物的体积约为22.4 L |
B. |
标准状况下, 1 L H2O电解后生成1 L H2 |
C. |
常温常压下,活泼金属从盐酸中置换出 1 mol H2时,转移的电子数为2 NA |
D. |
常温常压下, 1 mol He含有的核外电子数为4 NA |
下列说法中,正确的是
- A.常温常压下,活泼金属与盐酸反应置换生成1摩H2,发生转移的电子数为1NA
- B.22.4 L氢气中,一定含有2 mol氢原子
- C.在常温常压下,28g CO和N2的混合气体中含有的分子数为1NA
- D.80gNaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L
下列说法正确的是(NA表示阿伏加德罗常数)( )
A.标准状况下,以任意比例混合的甲烷和氧气混合物22.4 L,所含有的分子数为NA
B.标准状况下,1 L乙醇(C2H5OH)完全燃烧后,所生成气态产物的分子数为![]() NA
NA
C.常温常压下,活泼金属从盐酸中置换出1 mol H2,发生转移的电子数为2NA
D.常温常压下,1 mol氦气含有的核外电子数为4NA
查看习题详情和答案>>下列说法正确的是( )
| A.甲烷的标准燃烧热为-890.3KJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3KJ·mol-1 |
| B.500oC,30Mpa下,将0.5molN2和1.5H2置于密闭的容器中充分反应生成NH3(g),放热19.3KJ,其热化学方程式为: N2(g)+3H2(g) 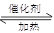 2NH3(g)△H=-38.6KJ·mol-1 2NH3(g)△H=-38.6KJ·mol-1 |
| C.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H﹥0 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 |