网址:http://m.1010jiajiao.com/timu3_id_212567[举报]
(1)将如图方框中的反应填补完整:
H吸附 ;O吸附 。
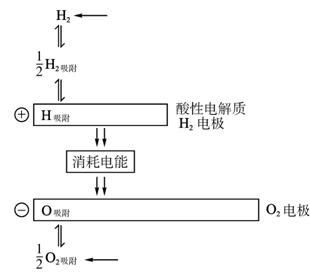
图1-6-5
(2)该电池反应为______________________________。
(3)人们将它用于航天飞行器上原因有两个:一是____________________,因此减轻质量就等于降低向太空发射的费用,与另一种绿色能源__________配合,可以使飞行器在空间停留的时间较长;二是______________________________,更可减少携带重量。
查看习题详情和答案>>(每空2分,共10分)依据事实,填空:
(1)已知某条件下可发生如下反应CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
(2)氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应式:正极: ;负极:
(3)某核素AZX的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20 ml才能把氯离子完全沉淀下来。则X的质量数为 ;
(4) 将甲烷和氧气的混合气体充入含有23.4 g Na2O2的密闭容器中,保持容器中温度为150 ℃,用电火花引燃充分反应后,压强为0 Pa,若将残留物溶于水,无气体逸出。此过程的总反应方程式为 。 查看习题详情和答案>>
(1)已知某条件下可发生如下反应CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
(2)氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应式:正极: ;负极:
(3)某核素AZX的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20 ml才能把氯离子完全沉淀下来。则X的质量数为 ;
(4) 将甲烷和氧气的混合气体充入含有23.4 g Na2O2的密闭容器中,保持容器中温度为150 ℃,用电火花引燃充分反应后,压强为0 Pa,若将残留物溶于水,无气体逸出。此过程的总反应方程式为 。
(每空2分,共10分)依据事实,填空:
(1) 已知某条件下可发生如下反应CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
|
化学键 |
C-H |
C=C |
C-C |
H-H |
|
键能(kJ/mol) |
414.4 |
615.3 |
347.4 |
435.3 |
则该反应的热化学方程式右边的ΔH= ;
(2)氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应式:正极: ;负极:
(3)某核素AZX的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20 ml才能把氯离子完全沉淀下来。则X的质量数为 ;
(4) 将甲烷和氧气的混合气体充入含有23.4 g Na2O2的密闭容器中,保持容器中温度为150 ℃,用电火花引燃充分反应后,压强为0 Pa,若将残留物溶于水,无气体逸出。此过程的总反应方程式为 。
查看习题详情和答案>>
(每空2分,共16分)依据事实,填空:
(1)在25℃、101kPa下,1g甲醇液体完全燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_____________________________
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_________________
(3)氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应式: 正极: ;负极:
(4)在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
该反应的反应方程式可表示为 ,平衡时Y气体的转化率 。
(5)某核素AZX的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20ml才能把氯离子完全沉淀下来。则X的质量数为 ;若X的核内中子数为20,则37 g XCl2中所含质子的物质的量 。
查看习题详情和答案>>