摘要:16.Cl2通入水中
网址:http://m.1010jiajiao.com/timu3_id_208562[举报]
Cl2通入水中发生如下反应:Cl2+H2O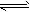 HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为
HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为
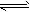 HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为
HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为 [ ]
A.加Na2CO3固体
B.加NaOH固体
C.加水
D.通入NH3气
查看习题详情和答案>>
B.加NaOH固体
C.加水
D.通入NH3气
|
Cl2通入水中发生如下反应:Cl2+H2O | |
A. |
加Na2CO3固体 |
B. |
加NaOH固体 |
C. |
加水 |
D. |
通入NH3 |
Cl2通入70℃的氢氧化钠水溶液中,能同时发生两个自身氧化还原反应(未配平):
NaOH+Cl2→NaCl+NaClO+H2O,NaOH+Cl2→NaCl+NaClO3+H2O.
反应完成后测得溶液中NaClO与NaClO3的数目之比为5:2,则该溶液中NaCl与NaClO的数目之比为( )
NaOH+Cl2→NaCl+NaClO+H2O,NaOH+Cl2→NaCl+NaClO3+H2O.
反应完成后测得溶液中NaClO与NaClO3的数目之比为5:2,则该溶液中NaCl与NaClO的数目之比为( )
查看习题详情和答案>>
Cl2通入70℃的NaOH水溶液中,发生氧化还原反应,反应完成后,测得溶液中NaClO与NaClO3的物质的量之比为4∶1,则:
(1)配平溶液中所发生反应的化学方程式:______Cl2+______NaOH——______NaCl+______
NaClO3+______NaClO+______
(2)反应中的氧化剂是________,氧化产物为________。
(3)此反应的离子方程式为________________________________________________。
(4)已知生成0.1 mol NaClO,反应中转移的电子总数是________mol,若溶液的体积正好为100 mL,则溶液中NaCl的物质的量浓度为________mol·L-1。
查看习题详情和答案>>