网址:http://m.1010jiajiao.com/timu3_id_208529[举报]
 (相对分子质量为180)。已知:阿司匹林药片中一般添加少量的辅料(都不溶于水,也不与NaOH反应)。某课外学习小组为检验阿司匹林有效成分的官能团并测定其在药片中的含量,进行了如下实验:
(相对分子质量为180)。已知:阿司匹林药片中一般添加少量的辅料(都不溶于水,也不与NaOH反应)。某课外学习小组为检验阿司匹林有效成分的官能团并测定其在药片中的含量,进行了如下实验: Ⅰ.验证乙酰水杨酸中具有羧基和酯的结构(—COOR)。
①将一片阿司匹林研碎后溶于水,静置,各取清液2 mL于两支洁净的试管中;
②向一支试管中加入____________,若观察到____________,即证明乙酰水杨酸中有羧基;
③向另一支试管中加入适量NaOH溶液,加热几分钟,冷却后逐滴滴入稀H2SO4,再向其中滴入FeCl3溶液,边加边振荡,若观察到溶液逐渐变为____________色,即证明乙酰水杨酸中具有酯的结构。
回答下列问题:
(1)将上述三处空白补充完整。
(2)实验中滴加稀H2SO4的作用是_____________________________________________。
Ⅱ.该学习小组设计了如下实验方案测定乙酰水杨酸在药片中的含量。
①称取阿司匹林样品m g;②将样品研碎,溶于V1 mL a mol·L-1 NaOH溶液中(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;③向锥形瓶中滴加几滴指示剂,用浓度为b mol·L-1的盐酸来滴定未反应的NaOH,消耗盐酸的体积为V2 mL。
回答下列问题:
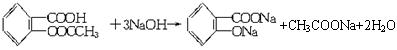
(1)阿司匹林中加入过量NaOH溶液并加热发生反应的化学方程式为____________;其中加热目的是____________________________________________________________。
(2)步骤③中若用酚酞作指示剂,如何判断滴定终点?________________________________
____________________________________________________________________。
(3)根据实验中记录的数据,阿司匹林药片中乙酰水杨酸质量分数的表达式为___________
_____________________________________________________________________。
查看习题详情和答案>>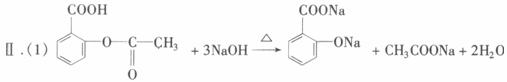
已知:①阿司匹林药片中一般添加少量的辅料(都不溶于水,也不与NaOH反应);②酚类物质与FeCl3溶液在弱酸性条件下能发生显色反应。
某课外学习小组为检验阿司匹林有效成分中的官能团并测定乙酰水杨酸在药片中的含量,进行了如下实验:
Ⅰ.验证乙酰水杨酸中具有羧基和酯的结构(—COOR)。
①将一片阿司匹林研碎后溶于水,静置,各取清液2 mL于两支洁净的试管中;
②向一支试管中加入_________,若观察到__________________,即证明乙酰水杨酸中有羧基;
③向另一支试管中加入适量NaOH溶液,加热几分钟,冷却后逐滴入稀H2SO4,再向其中滴入FeCl3溶液,边加边振荡,若观察到溶液逐渐变为_________色,即证明乙酰水杨酸中具有酯的结构。
回答下列问题:
(1)将上述三处空白补充完整。
(2)实验中滴加稀H2SO4的作用是__________________。
Ⅱ.该学习小组设计了如下实验方案测定乙酰水杨酸在药片中的含量:
①称取阿司匹林样品m g;
②将样品研碎,溶于V1 mL a mol·L-1 NaOH溶液(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;
③向锥形瓶中滴加几滴指示剂,用浓度为b mol·L-1的标准盐酸返滴未反应的NaOH,消耗盐酸的体积为V2 mL。
回答下列问题:
(1)阿司匹林中加入过量NaOH溶液并加热时发生反应的化学方程式为__________________;其中,加热的目的是__________________________________________。
(2)不能将阿司匹林溶解于水后直接用NaOH溶液进行滴定的原因是_____________________
____________________________________________________________________。
(3)根据实验中记录的数据,阿司匹林药片中乙酰水杨酸质量分数的表达式为_____________
_____________________________________________________________________。
查看习题详情和答案>>阿司匹林被誉为“百年新药”,阿司匹林药片的有效成分是乙酸水杨酸,它是一种白色晶体,微溶于水.其结构简式为: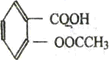 (相对分子质量为180).
(相对分子质量为180).
已知:阿司匹林药片种一般添加少量的辅料(都不溶于水,也不与![]() 反应);酚类物质与
反应);酚类物质与![]() 溶液再弱酸性质条件下能发生显色反应.
溶液再弱酸性质条件下能发生显色反应.
某课外学习小组为检验阿司匹林有效成分种的官能团并测定乙酰水杨酸再药片中的含量,进行了如下试验:
Ⅰ、验证乙酰水杨酸中具有羧基和酯的结构(-COOR).
①将一片阿司匹林研啐后溶于水,静置,各取清夜2![]() 于两支洁净的试管中;
于两支洁净的试管中;
②向一支试管中加入________,若观察到________,即证明乙酰水杨酸中有羧基;
③向另一支试管加入适量![]() 溶液,加热几分钟,冷却后逐滴滴入稀
溶液,加热几分钟,冷却后逐滴滴入稀![]() ,再向其中滴入
,再向其中滴入![]() 溶液,边加边振荡,若观察到溶液逐渐变为________色,即证明乙酰水杨酸中有酯的结构.
溶液,边加边振荡,若观察到溶液逐渐变为________色,即证明乙酰水杨酸中有酯的结构.
将上述三处空白补充完整
实验中滴加稀![]() 的作用是________
的作用是________
Ⅱ、该学习小组设计了如下试验方案测定乙酰水杨酸再药片中的含量;
①称取阿司匹林样品m![]() ;
;
②将样品研碎,溶于![]() a
a![]()
![]() 溶液(过量)并加热,出去辅料等不溶物,将所得溶液移入锥形瓶;
溶液(过量)并加热,出去辅料等不溶物,将所得溶液移入锥形瓶;
③向锥形瓶中滴加指示剂,用浓度为b![]() 的标准盐酸返滴未反应的
的标准盐酸返滴未反应的![]() ,消耗盐酸的体积未
,消耗盐酸的体积未![]() .
.
回答下列问题:
(1)阿司匹林中加入过量![]() 溶液并加热发生反应的化学方程式为:________;其中,加热的目的是________,
溶液并加热发生反应的化学方程式为:________;其中,加热的目的是________,
(2)不能将阿司匹林溶解于水后直接用![]() 溶液进行滴定的原因是________
溶液进行滴定的原因是________
(3)根据实验中记录的数据,阿司匹林药片中乙酰水杨酸质量分数的表达式为:________.
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是
(10分)A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示。请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀
①A中含有的金属元素为___________。
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,反应的化学反应方程式为____________________________________________________________。
(2)若A为固态非金属单质,A与X同周期,常温常压下C为白色固体,B分子中各原子最外层均为8电子结构。
①B的电子式为_____________。
②C与水剧烈反应,生成两种常见酸,反应的化学方程式为_______________________。
(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
①A中所含有的化学键是_____________。
②将4.48 L(标准状况下)X通入100mL 3 mol/L A的水溶液后,溶液中离子浓度由大到小的顺序为_______________________________________。
③自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为__________。
查看习题详情和答案>>