摘要:(一).选择题: 21.为了使鱼苗顺利运输.必须满足三个条件:(1)需要保持适量氧气,(2)使鱼苗呼出的二氧化碳及时排除,(3)防止细菌大量繁殖.则在远距离运输鱼苗的水中.最好加入适量下列物质中的( ) A.过氧化钠 B.氯水 C.石灰水 D.过氧化钙(CaO2) 22.由锌.铁.铝.镁四种金属中的两种组成的混合物10 g.与足量的盐酸反应产生的氢气在标准状况下为11.2 L.则混合物中一定含有的金属是( ) A. 锌 B.铁 C. 铝 D. 镁 23.下列说法正确的是( ) A.硫粉在过量的纯氧中燃烧可以生成大量的SO3 B.可以用澄清石灰水溶液鉴别SO2和CO2 C.SO2能使品红溶液.酸性KMnO4溶液褪色.但褪色原理不同 D.少量SO2通过浓CaCl2的溶液能生成白色沉淀
网址:http://m.1010jiajiao.com/timu3_id_206419[举报]
由银(74%)、铅(25%)、锑(1%)等制成的合金是一种优良的电镀新材料。对其中的银的分析,可采用络合滴定法,具体分析步骤概括如下:
试样![]() 沉淀(A)
沉淀(A)![]() 溶液(B)
溶液(B)![]() 溶液(C)
溶液(C)![]() 溶液(D)
溶液(D)
其中(I)加入HNO3(1:1),煮沸,再加入HCl(1:9),煮沸,过滤,依次用HCl(1:9)和水洗涤沉淀;(II)加入浓氨水,过滤,用5%氨水洗涤沉淀;(Ⅲ)加入氨水-氯化铵缓冲溶液(pH=10),再加入一定量的镍氰化钾固体;(IV)加入紫脲酸铵指示剂(简记为In),用乙二胺四乙酸二钠(简写为Na2H2Y)标准溶液滴定至近终点时,加入氨水10mL(为了使其终点明显),继续滴定至溶液颜色由黄色变为紫红色为终点。已知有关数据如下:
配合物 | [AgY]3- [NiY]2- [Ag(CN)2]- [Ni(CN)4]2- [Ag(NH3)2] + [Ni(NH3)6]2+ |
lgK稳 | 7.32 18.62 21.1 31.3 7.05 8.74 |
酸 | H4Y H3Y- H2Y2- HY3- |
lgKa | -2.0 -2.67 -6.16 -10.26 |
5-1写出A和D中Ag存在形体的化学式。
5-2写出第Ⅲ步骤的主反应方程式和第IV步骤滴定终点时的反应方程式。
5-3试样加HNO3溶解后,为什么要煮沸?加入HCl(1:9)后为什么还要煮沸?
5-4假定溶液C中Ag(I)的总浓度为0.010mol/L,游离NH3浓度为2mol/L,要求滴定误差控制在0.2%以内,试计算溶液C中Ni(II)总浓度至少为若干?
查看习题详情和答案>>21世纪的交通工具将采用由新一代无机非金属材料制成的无水冷发动机。这类材料中研究较多的要数化合物G。
(1)G可以由化合物E(含两种元素)与NH3反应制得,同时产生HCl气体。G的摩尔质量为140 g·mol-1,其中硅元素的质量分数为60%,另有元素Y。请推断:
①化合物G的化学式为____。
②上述制备G的反应中,1 mol NH3和0.75 mol E恰好完全反应,同时生成3mol HCl,则化合物E的分子式为 ____________________。
(2)为了使化合物G能成为新一代制造汽车发动机的材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐高温、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛纶”,化学通式可表示为Si6-xAlxOxY8-x。在接近于 1700℃时x的极限值约为4.0,在1400℃时x的极限值约为2.0,以保持整个化合物呈电中性。
①在不同温度时,“赛纶”中Y元素的化合价为____。
②在1400℃时,“赛纶”中硅元素的质量分数约为____。
查看习题详情和答案>>
(1)G可以由化合物E(含两种元素)与NH3反应制得,同时产生HCl气体。G的摩尔质量为140 g·mol-1,其中硅元素的质量分数为60%,另有元素Y。请推断:
①化合物G的化学式为____。
②上述制备G的反应中,1 mol NH3和0.75 mol E恰好完全反应,同时生成3mol HCl,则化合物E的分子式为 ____________________。
(2)为了使化合物G能成为新一代制造汽车发动机的材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐高温、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛纶”,化学通式可表示为Si6-xAlxOxY8-x。在接近于 1700℃时x的极限值约为4.0,在1400℃时x的极限值约为2.0,以保持整个化合物呈电中性。
①在不同温度时,“赛纶”中Y元素的化合价为____。
②在1400℃时,“赛纶”中硅元素的质量分数约为____。
某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质.
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙、丁四名同学进行Fe(OH)3胶体的制备
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL FeCl3饱和溶液,用玻璃棒搅拌,继续煮沸至溶液呈红褐色,停止加热.请评价该操作是否正确
②乙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确
(3)写出制备Fe(OH)3胶体的化学方程式:
(4)怎样检验制备的物质是否为胶体?
(5)取少量你制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是
(6)氢氧化铁胶体稳定存在的主要原因是
A.胶粒直径小于1nm B.胶粒带正电荷
C.胶粒作布朗运动 D.胶粒能透过滤纸.
查看习题详情和答案>>
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是
B
B
.A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙、丁四名同学进行Fe(OH)3胶体的制备
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL FeCl3饱和溶液,用玻璃棒搅拌,继续煮沸至溶液呈红褐色,停止加热.请评价该操作是否正确
不正确
不正确
.②乙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确
不正确
不正确
.(3)写出制备Fe(OH)3胶体的化学方程式:
FeCl3+3H2O═Fe(OH)3(胶体)+3HCl
FeCl3+3H2O═Fe(OH)3(胶体)+3HCl
.(4)怎样检验制备的物质是否为胶体?
利用丁达尔效应:让一束光线通过制得的Fe(OH)3胶体,从侧面观察到一条光亮的“通路”,说明已经制得胶体
利用丁达尔效应:让一束光线通过制得的Fe(OH)3胶体,从侧面观察到一条光亮的“通路”,说明已经制得胶体
.(5)取少量你制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是
产生红褐色沉淀
产生红褐色沉淀
,这种现象称为胶体的聚沉
聚沉
.(6)氢氧化铁胶体稳定存在的主要原因是
B
B
.A.胶粒直径小于1nm B.胶粒带正电荷
C.胶粒作布朗运动 D.胶粒能透过滤纸.
(2009?汕头模拟)为了使广东的天更蓝,空气更清新,目前我省某些城市对没有申领到“绿色”通行证的高污染车实行限行.高污染车排出的尾气中所含的污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有( )
查看习题详情和答案>>
 实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气.
实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气.(1)分别写出乙醇跟浓H2SO4反应生成①脱水生成CH2=CH2;②分子间脱水生成CH3CH2-O-CH2CH3;③SO2、CO2、水蒸气的化学方程式:①
CH3CH2OH
CH2═CH2↑+H2O
| 浓硫酸 |
| 170℃ |
CH3CH2OH
CH2═CH2↑+H2O
;②| 浓硫酸 |
| 170℃ |
2CH3CH2OH
CH3CH2OCH2CH3+H2O
| 浓硫酸 |
| 140℃ |
2CH3CH2OH
CH3CH2OCH2CH3+H2O
;③| 浓硫酸 |
| 140℃ |
CH3CH2OH+H2SO4
H2O+SO2↑+CO2↑
| 高温 |
CH3CH2OH+H2SO4
H2O+SO2↑+CO2↑
;| 高温 |
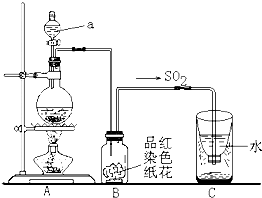
(2)二氧化硫是大气污染物之一,空气中的二氧化硫随雨水下降形成酸雨.如图实验装置,对酸雨的形成进行模拟并验证二氧化硫的部分性质,请回答:
①指出图中仪器a的名称:
分液漏斗
分液漏斗
.②B装置中淡红色纸花的颜色逐渐变褪去,说明SO2有
漂白
漂白
性.③反应结束后取出C装置中少量液体,滴加紫色石蕊试液后变
红
红
色.④实验完毕后.为了使多余的二氧化硫被充分吸收,C装置应如何改进?(用文字说明)
向C中加入过量的氢氧化钠溶液,震荡后静置
向C中加入过量的氢氧化钠溶液,震荡后静置
.