摘要:36:Fe + 2HCl == FeCl2 + H2↑ 37:3H2+ Fe2O3 高温 2Fe+3 H2O 38:2Al + 3H2SO4 ==Al2(SO4)3 + 3H2↑ 复习检测题(二)
网址:http://m.1010jiajiao.com/timu3_id_20537[举报]
36、黎明同学为了探究铝、铁、铜三种金属的活动性,他用铜丝、铁丝、铝丝和稀盐酸四种试剂,设计了以下只用一支试管,取一次盐酸的探究方案.
(1)请你帮助他完善下列的探究方案.
结论:金属活动性Al>Fe>Cu
写出①中反应得方程式:
将铝丝插入溶液前应进行得操作是
(2)甲同学看到黎明的方案后,认为只要再补充一个方案,就还能得出Al>Fe>H>Cu的结论,他认为要补充得实验是
(3)乙同学认为要得到活动性Al>Fe>H>Cu的结论,不必做实验,只要将黎明同学的实验中插入金属的顺序调整即可,调整后的金属插入顺序为
查看习题详情和答案>>
(1)请你帮助他完善下列的探究方案.
| 实验步骤 | 观察到的现象 |
| ①在试管中取少量盐酸,插入铁丝、充分反应 | |
| ②在①所得到的溶液中插入,充分反应 | 无明显现象 |
| ③在②所得到的溶液中插入,充分反应 |
写出①中反应得方程式:
Fe+2HCl=FeCl2+H2↑
.将铝丝插入溶液前应进行得操作是
用沙纸打磨除去铝丝表面的氧化铝
.(2)甲同学看到黎明的方案后,认为只要再补充一个方案,就还能得出Al>Fe>H>Cu的结论,他认为要补充得实验是
把铜丝插入盐酸中
.(3)乙同学认为要得到活动性Al>Fe>H>Cu的结论,不必做实验,只要将黎明同学的实验中插入金属的顺序调整即可,调整后的金属插入顺序为
铜、铁、铝
.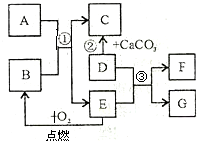 初中化学常见物质A-G有如右图所示的转化关系(部分反应条件及物质已略去),已知A、C所含元素相同且均为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位;F是最轻的气体.请回答下列问题:
初中化学常见物质A-G有如右图所示的转化关系(部分反应条件及物质已略去),已知A、C所含元素相同且均为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位;F是最轻的气体.请回答下列问题:(1)反应②的反应类型为
复分解反应
复分解反应
.(2)写出物质的名称:C为
二氧化碳
二氧化碳
;D为盐酸
盐酸
.(3)写出有关反应的化学方程式:
E在氧气中燃烧
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
;
| ||
反应①
4CO+Fe3O4
3Fe+4CO2
| ||
4CO+Fe3O4
3Fe+4CO2
;
| ||
反应③
Fe+2HCl=FeCl2+H2↑
Fe+2HCl=FeCl2+H2↑
.(4)F的一种用途是
用作燃料或冶炼金属等
用作燃料或冶炼金属等
.(5)小强同学在做中和反应实验时,向盛有40g 10%的氢氧化钠溶液的烧杯中逐滴加入稀盐酸,当恰好完全反应时,共滴加了36.5g稀盐酸.
①用氢氧化钠固体配制40g 10%的氢氧化钠溶液需要水
36
36
mL.(ρ水=1.0g/mL)②该中和反应的反应原理是
NaOH+HCl=NaCl+H2O
NaOH+HCl=NaCl+H2O
.③所加稀盐酸的溶质质量分数是
10%
10%
,反应后所得溶液中溶质的质量是5.85g
5.85g
.14、铁锈的主要成分是
查看习题详情和答案>>
Fe2O3
,为除去铁钉上的锈迹,某学生将带锈迹的铁钉放入过量的盐酸中,他首先看到锈迹溶解,溶液呈黄
色.这是因为(用化学方程式表示)Fe2O3+6HCl═2FeCl3+3H2O
;不一会儿,又看到溶液中有气体冒出
的现象,这是因为铁钉部分溶解(用化学方程式表示)Fe+2HCl═FeCl2+H2↑
.37、化学课外活动小组的同学们通过查阅资料得知:废弃的定影液中含有一定量的AgNO3.他们从摄影店收集到一些废弃的定影液,准备将其中的银以单质的形式全部回收.于是,他们进行了如下的实验活动:
【设计方案】①加入比银活动性强的金属单质;②除去金属混合物中的杂质.
【小组讨论】①选择加入的金属甲同学认为:向定影液中加入过量的铜粉,则得到银和铜的金属混合物;乙同学认为:向定影液中加入过量的铁粉,则得到银和铁的金属混合物.
你认为
②除去银粉中混有的金属,向上述所得的金属混合物中加入的试剂是
③进行实验:实验过程图示如下

在过滤操作中必须要用到的玻璃仪器是
产品验证:请你设计一种简单方法检验得到的银粉中是否含铁粉:
查看习题详情和答案>>
【设计方案】①加入比银活动性强的金属单质;②除去金属混合物中的杂质.
【小组讨论】①选择加入的金属甲同学认为:向定影液中加入过量的铜粉,则得到银和铜的金属混合物;乙同学认为:向定影液中加入过量的铁粉,则得到银和铁的金属混合物.
你认为
乙
(填“甲”或“乙”)同学的方案更合理,原因是铁比铜更容易被除去
;②除去银粉中混有的金属,向上述所得的金属混合物中加入的试剂是
稀盐酸(或稀硫酸)
,反应的化学方程式为Fe+2HCl═FeCl2+H2↑(或Fe+H2SO4═FeSO4+H2↑)
.③进行实验:实验过程图示如下

在过滤操作中必须要用到的玻璃仪器是
烧杯、漏斗、玻璃棒
,滤液A中溶质的化学式是Fe(NO3)2
; 产品验证:请你设计一种简单方法检验得到的银粉中是否含铁粉:
用磁铁接触,看得到的银粉是否被磁铁吸引或取少量固体滴入稀盐酸或稀硫酸,看是否有气泡放出等
.钢铁在生产和生活中有着广泛的用途,请回答下列问题.
(1)炼铁厂常以焦炭、赤铁矿石(主要成分是Fe2O3)、空气等为主要原材料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式
(2)每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟空气中的
(3)铁与盐酸反应的化学方程式为
(4)请写出一种防止铁生锈的方法
查看习题详情和答案>>
(1)炼铁厂常以焦炭、赤铁矿石(主要成分是Fe2O3)、空气等为主要原材料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(2)每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟空气中的
氧气
氧气
和水
水
共同作用的结果.(3)铁与盐酸反应的化学方程式为
Fe+2HCl═FeCl2+H2↑
Fe+2HCl═FeCl2+H2↑
.(4)请写出一种防止铁生锈的方法
在铁制品表面刷油漆
在铁制品表面刷油漆
.