摘要: 氨氧化制硝酸的反应如下: ①NH3+O2→NO+H2O ②NO+O2→NO2③NO2+H2O→HNO3+NO 如将氨全部氧化得2mol硝酸.下列哪个值是理论上需氧气的物质的量是 A.2mol B.3 mol C.4 mol D.5 mol
网址:http://m.1010jiajiao.com/timu3_id_204676[举报]
氨氧化制硝酸的反应如下(未配平):①NH3 + O2 →NO + H2O ②NO + O2 → NO2
③NO2+H2O→HNO3+NO,如将氨全部氧化得2mol硝酸,理论上需氧气的物质的量是( )
A、2mol B、3 mol C、4 mol D、5 mol
查看习题详情和答案>>
氨氧化制硝酸的反应如下(未配平):①NH3 + O2 →NO + H2O ②NO + O2 → NO2
③NO2+H2O→HNO3+NO,如将氨全部氧化得2mol硝酸,理论上需氧气的物质的量是( )
| A.2mol | B.3 mol | C.4 mol | D.5 mol |
氨氧化制硝酸的反应如下(未配平):①NH3 + O2 →NO + H2O ②NO + O2 → NO2
③NO2+H2O→HNO3+NO,如将氨全部氧化得2mol硝酸,理论上需氧气的物质的量是( )
③NO2+H2O→HNO3+NO,如将氨全部氧化得2mol硝酸,理论上需氧气的物质的量是( )
| A.2mol | B.3 mol | C.4 mol | D.5 mol |
氨氧化制硝酸的反应如下(未配平):①NH3 + O2 →NO + H2O ②NO + O2 → NO2 ③NO2+H2O→HNO3+NO,如将氨全部氧化得2mol硝酸,理论上需氧气的物质的量是
- A.2mol
- B.3 mol
- C.4 mol
- D.5 mol
 工业合成氨与制备硝酸一般可连续生产,流程如下:
工业合成氨与制备硝酸一般可连续生产,流程如下: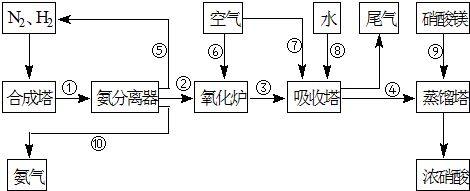
(1)合成塔中发生反应:N2(g)+3H2(g)?2NH3(g)+Q(Q>0).下表为不同温度下该反应的平衡常数.
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
(2)NH3和O2在铂系催化剂作用下从145℃就开始反应:
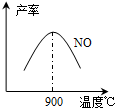
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+905kJ,不同温度下NO气体的产率如图所示.温度高于900℃时,NO气体产率下降的原因是
(3)吸收塔中反应为:3NO2+H2O?2HNO3+NO.从生产流程看,吸收塔中需要补充空气,其原因是
(4)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气.目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)→4NO(g)+CO2(g)+2H2O(g)+574kJ;
CH4(g)+4NO(g)→2N2(g)+CO2(g)+2H2O(g)+1160kJ.
则1mol甲烷直接将NO2还原为N2的热化学方程式为: