摘要:20."类比"是化学研究物质性质的基本方法之一.请运用类比法解答下列问题: 已知在一定条件下.过氧化钠几乎可与所有的常见气态非金属氧化物反应. 如:2Na2O2+2CO2=2Na2CO3+O2.Na2O2+CO=Na2CO3. (1)试分别写出Na2O2与SO3.SO2反应的化学方程式. , . (2)当1molSO3参加反应时,转移电子的物质的量为 mol. (3)通过比较可知:在氧化物中.当非金属元素处于 价时.其氧化物与过氧化钠反应就有O2 生成.
网址:http://m.1010jiajiao.com/timu3_id_204034[举报]
某校化学研究性学习小组的同学在学习了氨气的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?请你参与该小组的探究活动并回答下列问题:
(1)写出实验室制取氨气的化学方程式: .
(2)有同学类比排饱和食盐水收集氯气的方法,想用饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的? (填“能”或“否”)
(3)该小组某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性.
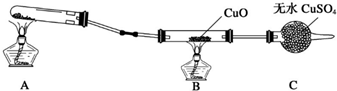
该装置上设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是 .
(4)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.写出氨气与CuO发生反应的化学方程式 .
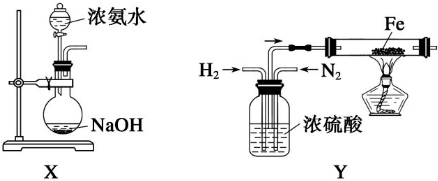
(5)若将改进后的装置中的A换成下图中的X,能否顺利完成实验? (填“能”或“否”).小组中的某同学将A换成了下图中的Y,结果无水CuSO4变蓝色,据此判断氨气与CuO发生了反应.你认为他的结论是否严谨? (填“是”或“否”).原因是 .
查看习题详情和答案>>
(1)写出实验室制取氨气的化学方程式:
(2)有同学类比排饱和食盐水收集氯气的方法,想用饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的?
(3)该小组某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性.

该装置上设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
(4)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.写出氨气与CuO发生反应的化学方程式
(5)若将改进后的装置中的A换成下图中的X,能否顺利完成实验?

下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25℃).
回答下列问题:
(1)由上表分析,若①CH3COOH ②HCO3-③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为 (须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式: ;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-) c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是 ;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3?H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式 .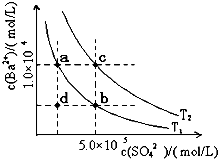
(6)Ⅰ.如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1 T2(填>、=、<),T2温度时Ksp(BaSO4)= ;
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理.若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次.[提示:BaSO4(s)+CO32-(aq)?BaCO3(s)+SO42- (aq)].
查看习题详情和答案>>
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- |
K1=4.31×10-7 K2=5.61×10-11 |
|
| C6H5OH | C6H5OH?C6H5O-+H+ | 1.1×10-10 | |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
|
| NH3?H2O | NH3?H2O?NH4++OH- | 1.76×10-5 | |
| BaSO4 | BaSO4?Ba2++SO42- | 1.07×10-10 | |
| BaCO3 | BaCO3?Ba2++CO32- | 2.58×10-9 |
(1)由上表分析,若①CH3COOH ②HCO3-③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为
(2)写出C6H5OH与Na3PO4反应的离子方程式:
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3?H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式

(6)Ⅰ.如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理.若使BaSO4中的SO42-全部转化到溶液中,需要反复处理
类比归纳是学习化学的重要方法,对如下类比的说法正确的是( )
| A、CO2、SO2都是酸性氧化物,都能使酸性高锰酸钾溶液褪色 | B、MgO、Al2O3都是高熔点离子化合物,熔化时都能导电 | C、CO2与SiO2化学式相似,则CO2与SiO2的物理性质也相似 | D、CuO、Fe2O3都是不溶于水的碱性氧化物,都是黑色粉末 |
硫代硫酸钠(Na2S2O3)可看成是一个S原子取代了Na2SO4中的一个O原子而形成.研究小组运用类比学习的思想,通过实验探究Na2S2O3的化学性质.
(1)他们提出如下猜想:猜想①:与BaCl2溶液反应有沉淀生成;猜想②:溶液呈中性,且不与酸反应;猜想③:无还原性,不能被氧化剂氧化.
他们提出上述猜想的依据是 .
(2)对上述猜想②、③,他们设计实验方案,并进行实验.请在答题卡上按下表格式完成相关的实验操作步骤、预期现象.请限选实验仪器与试剂:试管、玻璃棒、滴管、pH试纸:3mol?L-1H2SO4、新制氯水、1mol?L-1 BaCl2 溶液、Na2S2O3溶液、蒸馏水.
(3)小组同学为确证经操作三后Na2S2O3被氧化,提出如下实验方案 .
查看习题详情和答案>>
(1)他们提出如下猜想:猜想①:与BaCl2溶液反应有沉淀生成;猜想②:溶液呈中性,且不与酸反应;猜想③:无还原性,不能被氧化剂氧化.
他们提出上述猜想的依据是
(2)对上述猜想②、③,他们设计实验方案,并进行实验.请在答题卡上按下表格式完成相关的实验操作步骤、预期现象.请限选实验仪器与试剂:试管、玻璃棒、滴管、pH试纸:3mol?L-1H2SO4、新制氯水、1mol?L-1 BaCl2 溶液、Na2S2O3溶液、蒸馏水.
| 实验操作 | 实验现象或 预期实验现象 |
现象解释 (用离子方程式表示) |
结论 | |
| 猜想② | 操作一: |
溶液pH=8 | / | Na2S2O3溶液呈中性,能与酸反应,具有还原性,与Na2SO4的化学性质不相似. |
| 操作二: |
S2O32-+2H+=S↓+SO2↑+H2O | |||
| 猜想③ | 操作三: |