网址:http://m.1010jiajiao.com/timu3_id_203283[举报]
(1)研究小组首先排除了含有单质Al的可能性,加入的试剂是
A.硫酸 B.盐酸 C.氨水 D.氢氧化钠溶液
证明不含单质铝的现象是
(2)该混合物的组成基本确定为Fe、FeO、Al2O3.请以上述粉末为样品,验证其组成.限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/L盐酸、3% H2O2、3mol/LCuSO4、蒸馏水.
根据你设计的实验方案,在答题卡上按下表的格式写出空白部分的实验操作、预期现象和结论.
| 实验操作 | 预期现象和结论 |
| 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤. | 粉末减少,说明粉末可能含有Al2O3 |
| 步骤2:取少量步骤1的滤液于试管中,逐滴滴加3mol/L盐酸至过量. | 有白色沉淀产生然后沉淀又溶解 有白色沉淀产生然后沉淀又溶解 ,说明粉末中含有Al2O3. |
| 步骤3:将步骤1的滤渣转移到烧杯B中,加入足量3mol/L CuSO4,充分搅拌,过滤,洗涤. | 有红色固体生成,说明粉末中含有 Fe Fe . |
| 步骤4: 将步骤3的滤渣转移到烧杯C中, 加入足量3mol/L盐酸,静置,取上层清液, 滴加适量的双氧水,充分振荡后滴加KSCN 溶液. 将步骤3的滤渣转移到烧杯C中, 加入足量3mol/L盐酸,静置,取上层清液, 滴加适量的双氧水,充分振荡后滴加KSCN 溶液. |
固体部分溶解,溶液变血红色,说明粉 末中含有FeO 固体部分溶解,溶液变血红色,说明粉 末中含有FeO |
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg( b>a),则混合物中Cu2O的质量分数为
| 9(b-a) |
| a |
| 9(b-a) |
| a |
(5)实验小组欲利用该红色粉末制取较纯净的胆矾 (CuS04.5H20).经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH 如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验小组设计如下实验方案:
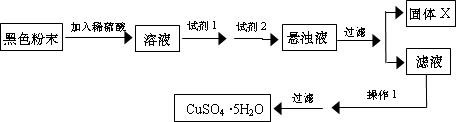
试回答:
①试剂I为
②固体X的化学式为
③操作I为
现有一份含有FeCl3和FeCl2固体的混合物,为测定各成分的含量进行如下两个实验:
实验1
①称取一定质量的样品,将样品溶解
②向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀
③将沉淀过滤、洗涤、干燥得到白色固体17.22g
实验2
①称取与实验1中相同质量的样品,将样品溶解
②向溶解后的溶液中,通入足量的Cl2
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀
④将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4g
根据实验回答下列问题:
(l)溶解过程中所用到的玻璃仪器有_____________________。
(2)实验室保存FeCl2溶液时通常会向其中加入少量试剂_________和_________。
(3)实验2中通入足量Cl2的目的是____________________________________。
涉及的化学反应的离子方程式是____________________________________。
(4)简述检验实验2的步骤④中沉淀已经洗涤干净的方法
_______________________________________________________________
_______________________________________________________________。
(5)加热FeCl3溶液,并将溶液蒸干时,通常不能得到FeCl3固体,请以平衡的观点解释其原因(方程式与文字相结合来说明)______________________________________。
(6)FeCl3溶液可以用于止血,主要是因为FeCl3溶液能使血液聚沉,这涉及到胶体的性质。以下关于胶体的说法不正确的是_____________(填写序号字母)。
A. 胶体粒子能透过滤纸,但不能透过半透膜
B. 胶体粒子具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
C. 只有胶体粒子能作布朗运动
D. 向Fe(OH)3胶体中滴加硫酸,会先出现红褐色沉淀,随后沉淀消失
E. 在蛋白质溶液中加入稀的CuSO4溶液,可使蛋白质盐析
(7)通过实验所得数据,计算得固体样品中FeCl3和FeCl2的物质的量之比为_________。
(8)实验室可以采用下列装置制取少量的FeCl3固体,已知FeCl3固体易潮解。(部分夹持仪器已略去)
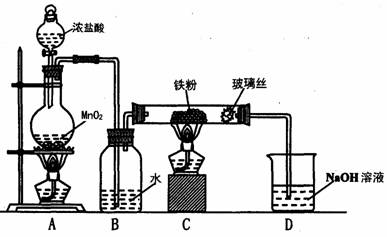
该装置存在不足,往往无法得到FeCl3固体,请你对该装置提出合理的改进措施
_______________________________________________________________。
查看习题详情和答案>>两组同学对铁及其化合物的性质进行探究。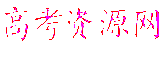
(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验。已知:
2Fe + 6H2SO4(浓) ![]() Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
①检查装置气密性后,将过量的铁屑和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时。
t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不
变。甲同学将收集到的气体体积与时间的关系粗略地表示为图2。
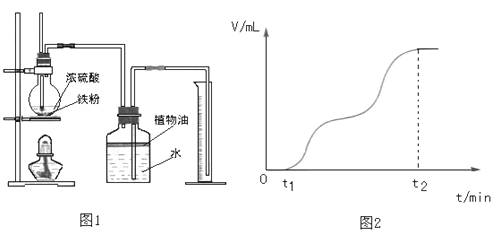
在0~t1时间段,铁屑表面没有气泡生成,说明铁在浓硫酸中发生了 ;t1~t2时间段,反应生成的气体是 。
②t2时,取少量反应液,先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现红色褪去。同学们对红色褪去的原因提出各自的假设。乙同学的假设是:溶液中的+3价铁被氧化为更高的价态。你的另一种假设是 ;为了验证你的假设,请设计一种简便的实验方案 。
(2)另一组同学对铁和稀硝酸的反应进行探究。他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+,则![]() 的取值范围是 ;为证实上述混合液中含有Fe2+,可以采取这样的做法:先取样,再加入 试剂,观察到溶液发生明显的颜色变化时,可以说明Fe2+的存在。
的取值范围是 ;为证实上述混合液中含有Fe2+,可以采取这样的做法:先取样,再加入 试剂,观察到溶液发生明显的颜色变化时,可以说明Fe2+的存在。
(12分)两组同学对铁及其化合物的性质进行探究。
(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验。
已知:2Fe + 6H2SO4(浓) ![]() Fe2(SO4)3+ 3SO2↑+ 6H2O。
Fe2(SO4)3+ 3SO2↑+ 6H2O。
请你参与探究并回答相关问题。
①检查装置气密性后,将过量的铁屑和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时。t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变。甲同学将收集到的气体体积与时间的关系粗略地表示为图2。在0~t1时间段,铁屑表面没有气泡生成,说明铁在浓硫酸中发生了 ;t1~t2时间段,反应生成的气体是 。
②t2时,取少量反应液,先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现红色褪去。同学们对红色褪去的原因提出各自的假设。乙同学的假设是:溶液中的+3价铁被氧化为更高的价态。
你的另一种假设是 ;为了验证你的假设,请设计一种简便的实验方案 。[
(2)另一组同学对铁和稀硝酸的反应进行探究。他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+,则a/b的取值范围是 ;为证实上述混合液中含有Fe2+,可以采取这样的做法:先取样,再加入 试剂,观察到溶液发生明显的颜色变化时,可以说明Fe2+的存在。
查看习题详情和答案>>