网址:http://m.1010jiajiao.com/timu3_id_203250[举报]

图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;
请填写下列空白:
(1)制取氯气时,通过分液漏斗向盛有二氧化锰固体的烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:
(3)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的酸电离出的H+使石蕊变色 氯气与水反应生成的酸电离出的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的次氯酸具有强氧化性将其漂白褪色 氯气与水反应生成的次氯酸具有强氧化性将其漂白褪色 |
在实验室可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
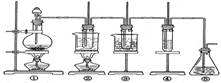
图中:①为氯气发生装置;②的试管里盛有15mL30%KOH 溶液.并置于水浴中; ③ 的试管里盛有15mL
8 % NaOH 溶液.并置于冰水浴中; ④ 的试管里加有紫色石蕊试液; ⑤ 为尾气吸收装置。请填写下列空白:
 (1)制取氯气时,在烧瓶里加人一定量的二氧化锰.通过___________(填写仪器名称)向烧瓶中加人适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_____________________(填写下列编号字母)的净化装置。
(1)制取氯气时,在烧瓶里加人一定量的二氧化锰.通过___________(填写仪器名称)向烧瓶中加人适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_____________________(填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件.二者的差异是_____________
反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是______(填写编号字母);从②的试管中分离出该晶体的方法是___________(填写实验操作名称)
(3)本实验中制取次氯酸钠的离子方程式是:________ ____
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为____色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | ____________________________________________ |
| 然后溶液从无色逐渐变为____色 | ____________________________________________ |
(14分)在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热 水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
⑴ 制取氯气时,在烧瓶里加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验室制Cl2的化学方程式 ;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
| A.碱石灰 | B.氢氧化钠溶液 | C.饱和食盐水 | D.浓硫酸 |
 06 mol。
06 mol。 其主要原因有:①_______________________________________________,
其主要原因有:①_______________________________________________,②__________________________________________________________________________。
⑶比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ;
② 。
反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是_______(填写编号字母);

从②的试管中分离出该晶体的方法是__________(填
 写实验操作名称)。
写实验操作名称)。⑷实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白。
实验 现象 现象 | 原因 |
| 溶液最初从紫色逐渐变为_______色 | 氯气与水反应 生成的H+使石蕊变色 生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | ____________________________ __________ __________ |
| 然后溶液从无色逐渐变为_______色 | ______________________ ________________ ________________ |
在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。 
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
⑴制取氯气时,在烧瓶里加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验室制Cl2的化学方程式 ;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
| A.碱石灰 | B.氢氧化钠溶液 | C.饱和食盐水 | D.浓硫酸 |
①______________________________________ _________,
②__________________________________________________________________________。
⑶ 比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ;
② 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。
①下图中符合该晶体溶解度曲线的是_______(填写编号字母);
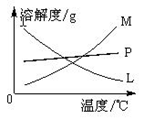
②从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。
⑷ 实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白。
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为_______色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | ______________________________________ |
| 然后溶液从无色逐渐变为_______色 | ______________________________________ |
在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
⑴制取氯气时,在烧瓶里加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验室制Cl2的化学方程式 ;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
⑵ 如果将过量二氧化锰与20 mL 12 mol·L-1的浓盐酸混合加热,充分反应后生成的氯气明显少于0. 06 mol。其主要原因有:
①______________________________________ _________,
②__________________________________________________________________________。
⑶ 比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ;
② 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。
①下图中符合该晶体溶解度曲线的是_______(填写编号字母);

②从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。
⑷ 实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白。
|
实验现象 |
原因 |
|
溶液最初从紫色逐渐变为_______色 |
氯气与水反应生成的H+使石蕊变色 |
|
随后溶液逐渐变为无色 |
______________________________________ |
|
然后溶液从无色逐渐变为_______色 |
______________________________________ |
查看习题详情和答案>>