摘要: 下列物质加入水中.对水的电离平衡无影响是的 ( ) A. CH3COOH B.HCl C. NaSO4 D.NH4Cl
网址:http://m.1010jiajiao.com/timu3_id_202116[举报]
已知A、B、C、D、E是化学中常见的物质,其中E是一种无色无味的液体,它们之间有如下反应关系.
(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式______.以下试剂中可用来区别C、D两种气体的是______.
①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是______当生成1molC时转移电子数是______.
(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是______.
(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是______.
①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小.
查看习题详情和答案>>
某校科技活动小组用镁粉、盐酸、醋酸设计以下实验,对两种酸分别与镁反应的速率和电离平衡理论进行研究,设计的实验装置如图所示(夹持固定装置已略去).
正确操作,记录得到下图2中部分实验数据.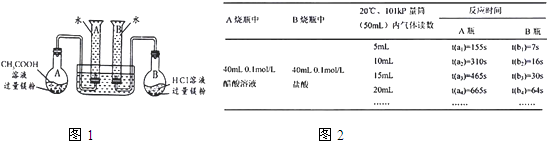
分析数据,观察实验装置图,回答下列问题:
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于
经小组研究后,稍作改进就可继续实验了;
(2)欲配置100mL实验所需浓度的盐酸,除烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是
(3)在实验数据中
①t(a1)远远大于t(b1)的原因为:
②由
(4)该实验得到什么结论?(回答出两点即可)
①
②
(5)通过实验判断,锌与稀盐酸制氢气时,若要减慢反应速率而不影响产生氢气的量,可以加入
查看习题详情和答案>>
正确操作,记录得到下图2中部分实验数据.

分析数据,观察实验装置图,回答下列问题:
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于
量筒口胶塞的使用,使得反应产生的H2无法进入量筒(当反应开始之后,会造成烧瓶或量筒的胶塞被气体强力推出而发生危险)
量筒口胶塞的使用,使得反应产生的H2无法进入量筒(当反应开始之后,会造成烧瓶或量筒的胶塞被气体强力推出而发生危险)
;经小组研究后,稍作改进就可继续实验了;
(2)欲配置100mL实验所需浓度的盐酸,除烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是
容量瓶(100mL)、玻璃棒
容量瓶(100mL)、玻璃棒
;(3)在实验数据中
①t(a1)远远大于t(b1)的原因为:
开始阶段醋酸溶液中的c(H+)远小于相同浓度的盐酸中的c(H+)
开始阶段醋酸溶液中的c(H+)远小于相同浓度的盐酸中的c(H+)
;②由
t(b3)-t(b2)>t(b2)-t(b1)或t(b3)>t(b1)+t(b2)
t(b3)-t(b2)>t(b2)-t(b1)或t(b3)>t(b1)+t(b2)
[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是强酸,不存在电离平衡;由t(a3)-t(a2)=t(a2)-t(a1)或t(a3)=t(a1)+t(a2)
t(a3)-t(a2)=t(a2)-t(a1)或t(a3)=t(a1)+t(a2)
[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.(4)该实验得到什么结论?(回答出两点即可)
①
相同物质的量浓度的盐酸、醋酸与金属反应时,盐酸开始反应速率大(过一段时间,醋酸与镁反应速率较盐酸的快)
相同物质的量浓度的盐酸、醋酸与金属反应时,盐酸开始反应速率大(过一段时间,醋酸与镁反应速率较盐酸的快)
;②
盐酸是强电解质,醋酸是弱电解质(存在电离平衡)
盐酸是强电解质,醋酸是弱电解质(存在电离平衡)
.(5)通过实验判断,锌与稀盐酸制氢气时,若要减慢反应速率而不影响产生氢气的量,可以加入
CH3COONa固体、水或NaCl溶液
CH3COONa固体、水或NaCl溶液
(填写两种不同作用原理的物质).(2012?山东模拟)已知A、B、C、D、E是化学中常见的物质,其中E是一种无色无味的液体,它们之间有如下反应关系.
(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式
①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是
(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是
(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是
①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小.
查看习题详情和答案>>

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.以下试剂中可用来区别C、D两种气体的是
| ||
①②④
①②④
.①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
当生成1molC时转移电子数是
| ||
2NA
2NA
.(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是
CaCl2、Ca(ClO)2
CaCl2、Ca(ClO)2
.(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是
②③
②③
.①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小.
已知A、B、C、D、E是化学中常见的物质,其中E是一种无色无味的液体,它们之间有如下反应关系.
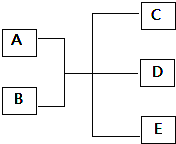
(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式______.以下试剂中可用来区别C、D两种气体的是______.
①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是______当生成1molC时转移电子数是______.
(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是______.
(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.
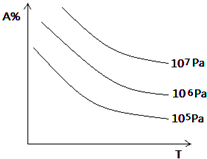
下列判断正确的是______.
①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小.
查看习题详情和答案>>

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式______.以下试剂中可用来区别C、D两种气体的是______.
①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是______当生成1molC时转移电子数是______.
(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是______.
(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是______.
①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小.
已知A、B、C、D、E是化学中常见的物质,其中E是一种无色无味的液体,它们之间有如下反应关系.
(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式 .以下试剂中可用来区别C、D两种气体的是 .
①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是 当生成1molC时转移电子数是 .
(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是 .
(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是 .
①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小. 查看习题详情和答案>>

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式 .以下试剂中可用来区别C、D两种气体的是 .
①酸性高锰酸钾溶液 ②溴水 ③澄清石灰水 ④品红溶液
(2)若A是一种黑色氧化物,B是一种常见的挥发性酸,反应时生成的C是气体,反应的离子方程式是 当生成1molC时转移电子数是 .
(3)若A是一种双原子分子,B是一种乳状物,得到的C、D混合物化学式分别是 .
(4)若aA(g)+bB(g)?cC(g)+dD(s)+eE(g)反应中A%随温度和压强的改变如下.

下列判断正确的是 .
①a+b<c+d+e ②正反应是吸热反应
③加入物质D对平衡没有影响 ④增大加强时平衡左移,平衡常数减小. 查看习题详情和答案>>