摘要:25. 实验室欲配制0.5 mol/L的NaOH溶液500 mL: (1)配制溶液时.一般可以分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 其正确的操作顺序为 . (2)某同学欲称量NaOH的质量.他先用托盘天平称量烧杯的质量.天平平衡后的状态如图.由图中可以看出.该同学在操作时的一个错误是 . 烧杯的实际质量为 . (3)使用容量瓶前必须进行的一步操作是 . (4)在配制过程中.其他操作都正确的.下列操作会引起误差偏高的是 ①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面 ③容量瓶不干燥.含有少量蒸馏水 ④定容时俯视标线 ⑤定容时仰视标线 ⑥定容后塞上瓶塞反复摇匀.静置后.液面低于刻度线.再加水至刻度线.
网址:http://m.1010jiajiao.com/timu3_id_200755[举报]
下列关于实验原理或操作的叙述,正确的是( )
| A、实验室欲用480mL0.2mol?L-1H2SO4溶液,可用500mL容量瓶配制 | B、用图所示装置测定NaOH溶液的浓度 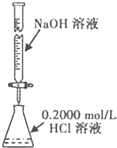 | C、铜与浓硫酸反应时,用蘸有浓溴水的棉花放在导管口吸收多余的气体 | D、制取NaCl晶体,可往烧杯中加入NaCl溶液,加热、蒸干 |
实验室欲配制80mL 0.2mol/LNa2CO3溶液,下列说法正确的是( )
| A、需在托盘天平上称取约1.7克Na2CO3固体 | B、洗涤烧杯后的溶液用玻璃棒引流到容量瓶中 | C、洗涤2-3次后,用蒸馏水沿玻璃棒注入容量瓶至刻度线 | D、某同学采用仰视的方式定容,则配出的溶液浓度偏高 |
实验室欲配制480mL浓度为0.1mol?L-1的Na2CO3溶液,下列操作可以实现的是( )
| A、称量5.3g Na2CO3固体溶于480mL水配制成溶液 | B、称量5.3g Na2CO3固体溶于水配制成0.5L溶液 | C、称量5.3g Na2CO3?10H2O晶体溶于水配制成0.5L溶液 | D、称量5.3g Na2CO3?10H2O晶体溶于0.5L水配制成溶液 |