网址:http://m.1010jiajiao.com/timu3_id_200328[举报]
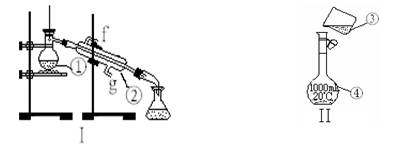
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
⑴写出下列仪器的名称:
①____________;②_____________;④__________;
⑵仪器①~④中,使用时必须检查是否漏水的有______。(填序号)
⑶若利用装置I分离四氯化碳和乙醇的混合物,还缺少的仪器是_________,将仪器补充完整后进行的实验操作的名称为_____________ 。现需配制250 mL 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是______________、_________________ 。
查看习题详情和答案>>
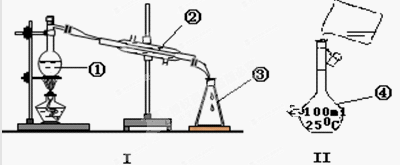
(13分)掌握仪器的名称、组装及使用方法是中学化学实验的基础,右下图为两套实验装置。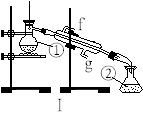

⑴写出下列仪器的名称:
① ;② ;④ ;
⑵仪器①~④中,使用时必须检查是否漏水的有 。(填序号)
⑶若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有 ;将仪器补充完整后进行的实验操作的名称为: 。现需配制250 ml 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是 。
(11分)掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
⑴写出下列仪器的名称:
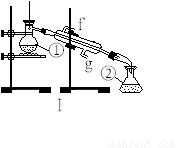
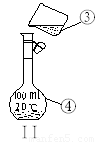
①____________;②____________;④____________;
⑵仪器①~④中,使用时必须检查是否漏水的有__________ 。(填序号)
⑶若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有________________,将仪器补充完整后进行的实验操作的名称为;_________________ 。现需配制250 ml 0.2 mol/L NaCL溶液,装置II是某同学转移溶液的示意图,图中的错误是__________________
__________________________________________________________________(指出两处)。
查看习题详情和答案>>
(11分)掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
⑴写出下列仪器的名称: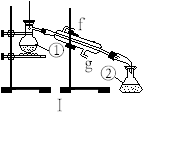
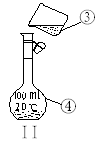
①____________;②____________;④____________;
⑵仪器①~④中,使用时必须检查是否漏水的有__________ 。(填序号)
⑶若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有________________,将仪器补充完整后进行的实验操作的名称为;_________________ 。现需配制250 ml 0.2 mol/L NaCL溶液,装置II是某同学转移溶液的示意图,图中的错误是__________________
__________________________________________________________________(指出两处)。