摘要:26. Ⅰ.下图是制取纯净.干燥的Cl2并进行有关Cl2性质实验的装置.装置中的C. D瓶均为洗气瓶.E瓶中放有干燥的红布条,F管中有铜丝,G瓶为集气瓶,H为尾气吸收装置. ① ② 试回答: (1)装置①发生反应的化学方程式为 . (2)C中的试剂是 .作用是 ,D中的试剂是 ,作用是 . Ⅱ.已知Cl2+H2OHCl+HClO.为了探究HClO的漂白性.某同学设计了如下的实验. (1)通入Cl2后.从集气瓶A中干燥的红色布条的现象可得出的结论是 , 从集气瓶B中湿润的红色布条的现象可得出的结论是 . (2)为了确认是HClO使湿润的红色布条褪色.你认为还应增加的实验是 . (3)烧杯中发生反应的化学方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_199791[举报]
下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中D瓶中放有干燥红色布条;E中为铜网,E右端出气管口附近为石棉球。
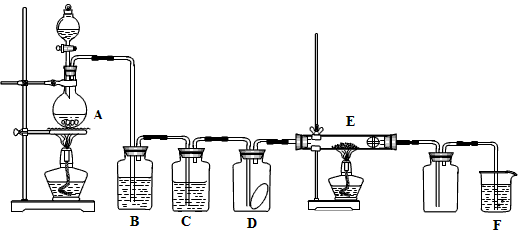
试回答:
(1)A中发生反应的方程式为________________________________;
(2)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,其作用是______________;
(3)C中盛放的试剂为_____________;
(4)E中所发生反应的方程式为______________________________。
(5)F中应加入的试剂为__________,其作用是____________________。
(6)若A中有14.6g HCl 被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量为________g。
查看习题详情和答案>>
(1)A中发生反应的方程式为________________________________;
(2)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,其作用是______________;
(3)C中盛放的试剂为_____________;
(4)E中所发生反应的方程式为______________________________。
(5)F中应加入的试剂为__________,其作用是____________________。
(6)若A中有14.6g HCl 被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量为________g。
下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置.其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放在脱脂棉.

试回答:
(1)A中所放试剂为________,B中所放试剂为________,此反应氧化剂是________;
(2)C中试剂是________;D中试剂的作用是________.
(3)E中现象是________;F中现象是________,其反应的化学方程式为________;F管中脱脂棉的作用是________;
(4)H中试剂为________,反应的离子方程式为________.
(5)整套装置中有两处用酒精灯加热,两处酒精灯点燃的先后顺序是________.
(6)若A中有14.6 gHCl被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量为________g.
工业上将纯净干燥的氯气通入到物质的量浓度为0.375mol/LNaOH溶液中得到漂水.某同学想在实验室探究Cl2性质并模拟制备漂水,如图是部分实验装置.已知KMnO4与盐酸溶液反应可以制取Cl2.
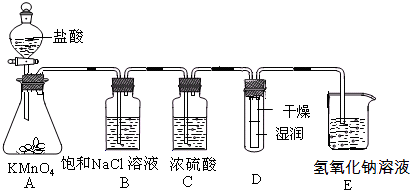
(1)配制物质的量浓度为0.375mol/LNaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和______.
(2)浓硫酸的作用是______.
(3)装置E中发生化学反应的离子方程式为______.
(4)装置B中饱和NaCl溶液可用于除去Cl2中的HCl气体,已知氯气与水的反应是一个可逆反应,请简述饱和NaCl溶液除去Cl2中HCl气体的原理(用离子方程式表示和文字说明)______.
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色.该同学认为Cl2的密度比空气大,可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的.请判断该解释是否合理______,并分析产生上述实验现象的原因______;如需改进,请简述设计方案______(若认为合理.则此问可不作答).
(6)氯元素含量为10%的漂水溶液355g,其中含NaClO的物质的量为______mol.
查看习题详情和答案>>
工业上将纯净干燥的氯气通入到物质的量浓度为0.375mol/LNaOH溶液中得到漂水.某同学想在实验室探究Cl2性质并模拟制备漂水,如图是部分实验装置.已知KMnO4与盐酸溶液反应可以制取Cl2.
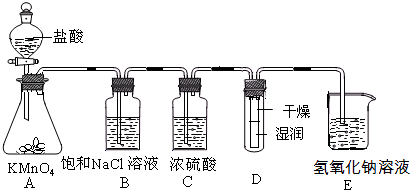
(1)配制物质的量浓度为0.375mol/LNaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和______.
(2)浓硫酸的作用是______.
(3)装置E中发生化学反应的离子方程式为______.
(4)装置B中饱和NaCl溶液可用于除去Cl2中的HCl气体,已知氯气与水的反应是一个可逆反应,请简述饱和NaCl溶液除去Cl2中HCl气体的原理(用离子方程式表示和文字说明)______.
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色.该同学认为Cl2的密度比空气大,可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的.请判断该解释是否合理______,并分析产生上述实验现象的原因______;如需改进,请简述设计方案______(若认为合理.则此问可不作答).
(6)氯元素含量为10%的漂水溶液355g,其中含NaClO的物质的量为______mol.
查看习题详情和答案>>

(1)配制物质的量浓度为0.375mol/LNaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和______.
(2)浓硫酸的作用是______.
(3)装置E中发生化学反应的离子方程式为______.
(4)装置B中饱和NaCl溶液可用于除去Cl2中的HCl气体,已知氯气与水的反应是一个可逆反应,请简述饱和NaCl溶液除去Cl2中HCl气体的原理(用离子方程式表示和文字说明)______.
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色.该同学认为Cl2的密度比空气大,可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的.请判断该解释是否合理______,并分析产生上述实验现象的原因______;如需改进,请简述设计方案______(若认为合理.则此问可不作答).
(6)氯元素含量为10%的漂水溶液355g,其中含NaClO的物质的量为______mol.
工业上将纯净干燥的氯气通入到物质的量浓度为0.375mol/LNaOH溶液中得到漂水.某同学想在实验室探究Cl2性质并模拟制备漂水,如图是部分实验装置.已知KMnO4与盐酸溶液反应可以制取Cl2.

(1)配制物质的量浓度为0.375mol/LNaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 .
(2)浓硫酸的作用是 .
(3)装置E中发生化学反应的离子方程式为 .
(4)装置B中饱和NaCl溶液可用于除去Cl2中的HCl气体,已知氯气与水的反应是一个可逆反应,请简述饱和NaCl溶液除去Cl2中HCl气体的原理(用离子方程式表示和文字说明) .
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色.该同学认为Cl2的密度比空气大,可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的.请判断该解释是否合理 ,并分析产生上述实验现象的原因 ;如需改进,请简述设计方案 (若认为合理.则此问可不作答).
(6)氯元素含量为10%的漂水溶液355g,其中含NaClO的物质的量为 mol. 查看习题详情和答案>>

(1)配制物质的量浓度为0.375mol/LNaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 .
(2)浓硫酸的作用是 .
(3)装置E中发生化学反应的离子方程式为 .
(4)装置B中饱和NaCl溶液可用于除去Cl2中的HCl气体,已知氯气与水的反应是一个可逆反应,请简述饱和NaCl溶液除去Cl2中HCl气体的原理(用离子方程式表示和文字说明) .
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色.该同学认为Cl2的密度比空气大,可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的.请判断该解释是否合理 ,并分析产生上述实验现象的原因 ;如需改进,请简述设计方案 (若认为合理.则此问可不作答).
(6)氯元素含量为10%的漂水溶液355g,其中含NaClO的物质的量为 mol. 查看习题详情和答案>>