摘要:14.将3.5g Fe.Mg合金投入到一定量的硝酸中.金属与硝酸恰好完全反应.共收集到标准状况下的气体VL.若向反应后的溶液中加入足量的氢氧化钠溶液.待金属元素全部沉淀后.再将沉淀过滤.洗净.干燥后称得质量为8.6g.则收集到的气体体积V值可能为 A.1.12 B.5.34 C.6.72 D.8.23
网址:http://m.1010jiajiao.com/timu3_id_199611[举报]
(2010?卢湾区二模)将2.4g Fe、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g.则收集到的气体体积V的值可能为( )
查看习题详情和答案>>
将2.4g Fe、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g。则收集到的气体体积V的值可能为( )。
A.0.896 B.1.10 C. 1.69 D. 2.24
查看习题详情和答案>>
将2.4g Fe、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g。则收集到的气体体积V的值可能为( )。
A.0.896 B.1.10 C. 1.69 D.2.24
查看习题详情和答案>>
将2.4g Fe、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g.则收集到的气体体积V的值可能为
- A.0.896
- B.1.10
- C.1.69
- D.2.24
 (2010?西城区一模)甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系.甲+乙→丙+丁
(2010?西城区一模)甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系.甲+乙→丙+丁(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水.
①若甲为块状固体,丙为可燃性气体,其分子内既含有极性键又含有非极性键.则丙的电子式是


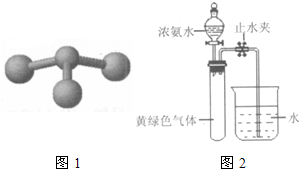
②若甲是由N和Cl元素组成的化合物,其分子结构模型
如图1所示,丙具有漂白性.则甲中Cl元素的化合价是
+1
+1
.(2)转化关系中所涉及的反应为氧化还原反应,且乙为水.
①若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.②若丙和丁都可在一定条件下还原CuO,此反应的化学方程式是
C+H2O(g)
CO+H2
| ||
C+H2O(g)
CO+H2
.
| ||
③若甲是由N和O元素组成的气态物质,呈红棕色.将3.36g Fe加到一定量丙溶液中,收集到1.12L气体丁(已折算为标准状况),则反应的离子方程式是
6Fe+20HNO3=3Fe(NO3)2+3Fe(NO3)3+5NO+10H2O
6Fe+20HNO3=3Fe(NO3)2+3Fe(NO3)3+5NO+10H2O
.(3)Hofmann依据上述转化关系测定氨分子的组成.现用如图2所示的装置进行实验,打开分液漏斗的活塞,滴下浓氨水,至不再反应为止;关闭分液漏斗的活塞,待恢复到室温,打开止水夹,试管内液面上升至
| 2 |
| 3 |
①滴下浓氨水一段时间后,试管内发生反应的化学方程式是
8NH3+3C12=N2+6NH4Cl
8NH3+3C12=N2+6NH4Cl
.②证明试管内“不再反应”的实验操作和现象是
待产生的大量白烟沉降后,继续滴加浓氨水,不再产生白烟
待产生的大量白烟沉降后,继续滴加浓氨水,不再产生白烟
.