摘要:33. 在某石灰石样品中含有少量二氧化硅杂质.10 g该样品与50 mL 4 mol/L盐酸充分反应后.得到2128 mL CO2.计算: (1)石灰石样品中SiO2的质量分数, (2)中和多余盐酸所需0.5 mol/L NaOH溶液的体积.
网址:http://m.1010jiajiao.com/timu3_id_198336[举报]
过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
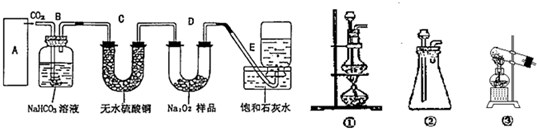
(1)请写出过氧化钠与二氧化碳反应的化学方程式,并标明电子转移的方向和数目:
 ;
;
(2)A中制取CO2的装置,应从下列图①、②、③中选哪个图:
(3)B装置的作用是
(4)为了检验E中收集到的气体,在取出集气瓶后,用
(5)若E中石灰水出现轻微白色浑浊,请说明原因:
(6)当D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?
(7)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值
查看习题详情和答案>>

(1)请写出过氧化钠与二氧化碳反应的化学方程式,并标明电子转移的方向和数目:


(2)A中制取CO2的装置,应从下列图①、②、③中选哪个图:
②
②
;(3)B装置的作用是
除CO2中的HCl
除CO2中的HCl
;(4)为了检验E中收集到的气体,在取出集气瓶后,用
带火星
带火星
的木条伸入集气瓶内,木条会出现复燃
复燃
;(5)若E中石灰水出现轻微白色浑浊,请说明原因:
未反应的二氧化碳与石灰水反应所致
未反应的二氧化碳与石灰水反应所致
;(6)当D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?
由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸
由于生成氧气的量减少,E中可能会因二氧化碳与石灰水反应而倒吸
;(7)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值
小
小
(大或小),相差约30
30
mL(取整数值,所用数据均在标准状况下测定),这是由于Na2O2可能含有其它杂质;D装置可能有氧气未被排出
Na2O2可能含有其它杂质;D装置可能有氧气未被排出
.
已知二氧化硅与C在高温下有发生两种反应的可能:
![]()
取某石英样品(杂质高温下不与C反应)
(1)原样品中SiO2的质量分数是多少?
(2)如有5.00 t这种样品,理论上最多可制得99.9%的高纯硅多少吨?
查看习题详情和答案>>已知二氧化硅与C在高温下有发生两种反应的可能:SiO2+2C![]() Si+2CO↑,SiO2+3C
Si+2CO↑,SiO2+3C![]() SiC+2CO↑.
SiC+2CO↑.
取某石英样品(杂质高温下不与C反应)4.00 g,与足量的C混合共热,把生成的气体完全燃烧后全部通入含Ca(OH)24.44 g的饱和石灰水中,恰好使生成的沉淀又重新溶解.试求:
(1)原样品中SiO2的质量分数是多少?
(2)如有5.00 t这种样品,理论上最多可制得99.9%的高纯硅多少吨?
已知二氧化硅与C在高温下有发生两种反应的可能:
![]()
取某石英样品(杂质高温下不与C反应)4.00 g,与足量的C混合共热,把生成的气体完全燃烧后全部通入含Ca(OH)24.44 g的饱和石灰水中,恰好使生成的沉淀又重新溶解。试求:
(1)原样品中SiO2的质量分数是多少?
(2)如有5.00 t这种样品,理论上最多可制得99.9%的高纯硅多少吨?
查看习题详情和答案>>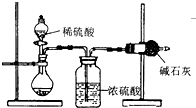 测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:
测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:I.吸收法
如图所示:
(1)根据实验装置图分析,在每次实验过程中所进行的称量操作至少要进行
4
4
次,且第一次称量操作的对象是称量干燥烧瓶的质量
称量干燥烧瓶的质量
.(2)若重复测定了三次,得到Na2CO3的质量分数的数据存在较大的偏差,产生偏差的原因可能是
ACD
ACD
(填序号).A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.用了稀硫酸与样品反应
C.加入稀硫酸的量不足,则可能造成误差
D.反应完成后,装置中仍存有二氧化碳,没有被碱石灰吸收
除上述原因外,从装置看还有一个重要原因是
装置外的空气中的水蒸气和二氧化碳被碱石灰吸收
装置外的空气中的水蒸气和二氧化碳被碱石灰吸收
.II.滴定法
称取样品m g,配制成500mL溶液.从中取出25mL加入足量的BaCl2溶液振荡,滴加2~3滴酚酞,用a mol/L标准盐酸滴定,至终点时消耗盐酸v mL.
(1)该同学加入足量的BaCl2溶液后未将BaCO3过滤就滴定,有人认为在滴定中BaCO3会转化为Ba(HCO3)2,消耗盐酸.你认为要过滤吗?
否
否
(填“是”或“否”),理由是:用酚酞做指示剂到终点时溶液呈微弱的碱性,BaCO3不反应
用酚酞做指示剂到终点时溶液呈微弱的碱性,BaCO3不反应
(若填“是”,不需答).(2)判断滴定终点到达的依据是
当滴入最后一滴盐酸时,溶液立即由浅红色变化为无色,且半分钟内颜色不变化
当滴入最后一滴盐酸时,溶液立即由浅红色变化为无色,且半分钟内颜色不变化
.Ⅲ.沉淀法
称取样品m g,并溶解加过量Ba(NO3)2溶液,过滤、洗涤、烘干,称量得固体n g.
(1)混合物中碳酸钠的质量分数为(用m、n表示)
| 106n |
| 197m |
| 106n |
| 197m |
(2)洗涤沉淀的操作要点是
用玻璃棒向过滤器中的沉淀加水至淹没,静置使水滤出,并重复2-3次
用玻璃棒向过滤器中的沉淀加水至淹没,静置使水滤出,并重复2-3次
.(3)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用Ba(NO3)2溶液而不用Ca(NO3)2溶液的原因是
Ca(OH)2微溶
Ca(OH)2微溶
;测定CO32-的量,若使用Ba(OH)2溶液而不用Ca(OH)2溶液,结果将具有更高的精确度,原因BaCO3相对分子质量大,相对误差小
BaCO3相对分子质量大,相对误差小
.