摘要:8.元素A.B.C都是短周期无素.它们的原子序数大小顺序是:A<B<C.A元素原子次外层电子数为最外层电子数的l/2,B元素原子次外层电子数是最外层电子数的2倍.B与C可形成共价化合物BC4.则下列有关说法正确的是 A.它们的单质通常情况下都不能导电 B.它们的最高价氧化物都能与H2O反应 C.它们的原子半径大小顺序是A>B>C D.它们的最高价氧化物对应水化物的酸性由强到弱的顺序为C>A>B
网址:http://m.1010jiajiao.com/timu3_id_197646[举报]
元素A、B、C都是短周期无素,它们的原子序数大小顺序是:A<B<C,A元素原子次外层电子数为最外层电子数的1/2;B元素原子次外层电子数是最外层电子数的2倍,B与C可形成共价化合物BC4,则下列有关说法正确的是
- A.它们的单质通常情况下都不能导电
- B.它们的最高价氧化物都能与H2O反应
- C.它们的原子半径大小顺序是A>B>C
- D.它们的最高价氧化物对应水化物的酸性由强到弱的顺序为C>A>B
|
元素A、B、C都是短周期无素,它们的原子序数大小顺序是:A<B<C,A元素原子次外层电子数为最外层电子数的1/2;B元素原子次外层电子数是最外层电子数的2倍,B与C可形成共价化合物BC4,则下列有关说法正确的是 | |
| [ ] | |
A. |
它们的单质通常情况下都不能导电 |
B. |
它们的最高价氧化物都能与H2O反应 |
C. |
它们的原子半径大小顺序是A>B>C |
D. |
它们的最高价氧化物对应水化物的酸性由强到弱的顺序为C>A>B |
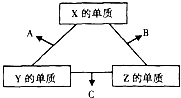 X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题:
X、Y、Z三种短周期元素,它们的原子序数之和为16.在常温下,X、Y、Z三种元素的常见单质都是无色气体,它们在适当条件下可发生如图所示的转化.已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数少一个.请回答下列问题:(1)X元素在周期表中的位置是
第二周期VIA族
第二周期VIA族
.Y的原子序数为7
7
.(2)X的单质与Z的单质可制成新型的化学电源,该电源被称为
氢氧燃料电池
氢氧燃料电池
.(3)A的化学式为
NO
NO
.(4)已知Y的单质与Z的单质在适当催化剂和高温、高压条件下,生成C的反应是可逆反应,写出该反应的化学方程式
N2+3H2
2NH3
| 高温、高压 |
| 催化剂 |
N2+3H2
2NH3
.| 高温、高压 |
| 催化剂 |
X、Y、Z三种短周期元素,它们的原子序数之和等于16,X2、Y2、Z2在常温下都是无色气体,它们均为工业合成某化工产品的重要原料,其流程如下:

已知:①一定条件下,X2与Y2能反应生成A,X2与Z2能反应生成B;
②B和C分子均为常见的10电子微粒.
请回答下列问题:
(1)X元素在周期表中的位置是
(2)X2与Z2可制成新型化学电源(KOH溶液作电解质溶液),两个电极均由多孔石墨制成,通入的气体在电极表面放电,负极电极反应式为
(3)化合物B吸收C后形成的溶液pH
(4)写出由C生成A和B的化学方程式
查看习题详情和答案>>

已知:①一定条件下,X2与Y2能反应生成A,X2与Z2能反应生成B;
②B和C分子均为常见的10电子微粒.
请回答下列问题:
(1)X元素在周期表中的位置是
第二周期第ⅥA族
第二周期第ⅥA族
.(2)X2与Z2可制成新型化学电源(KOH溶液作电解质溶液),两个电极均由多孔石墨制成,通入的气体在电极表面放电,负极电极反应式为
H2+2OH--2e-═2H2O
H2+2OH--2e-═2H2O
.(3)化合物B吸收C后形成的溶液pH
>
>
7(填“大于”、“小于”或“等于”),其原因是(用离子方程式表示)NH3?H2O?NH4++OH-
NH3?H2O?NH4++OH-
.(4)写出由C生成A和B的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
