摘要:某进行无土栽培试验的实验室须要配制两份成分完全相同的某营养液.其配方如下表. KCl K2SO4 ZnSO4 0.3mol 0.2mol 0.1mol 但实验员配完第一分溶液时发现.实验室的ZnSO4已经用完了.锌盐中只剩下了硝酸锌(Zn(NO3)2).氯化锌(ZnCl2). 请为实验员想想如何都能配得第二份营养液. (写出至少两种可行的途径)
网址:http://m.1010jiajiao.com/timu3_id_197411[举报]
(17分)实验室可利用甲醇、空气、铜制备甲醛,关于甲醇和甲醛的沸点和水溶液性见下表:
| 沸点/℃ | 水溶性 | |
| 甲醇 | 65 | 与水相溶 |
| 甲醛 | ―21 | 与水相溶 |
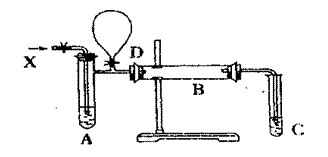
下图是某位同学设计的实验装置,其中D处的气球在反应结束时使用。
![]()
 |
![]()
![]()
![]()
![]()
![]()
![]()
![]() 请回答:
请回答:
![]() (1)通往A试管的X是 ,B管中发生反应的化学方程式为 。
(1)通往A试管的X是 ,B管中发生反应的化学方程式为 。
![]() (2)C试管中装入的试剂是 ,管内收集到的物质有 。
(2)C试管中装入的试剂是 ,管内收集到的物质有 。
![]() (3)对装置中的A、B、C还需要采取什么措施(实验室提供用品),才能使试验顺利进行:对A是 ;对B是 ;对C是 。
(3)对装置中的A、B、C还需要采取什么措施(实验室提供用品),才能使试验顺利进行:对A是 ;对B是 ;对C是 。
![]() (4)反应结束时,对D处气球的操作是 。
(4)反应结束时,对D处气球的操作是 。
![]()
 (2012?长沙模拟)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验.
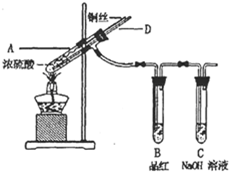
(2012?长沙模拟)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验.【实验1】铜与浓硫酸反应,实验装置如图所示.
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面.
(1)装置A中发生反应的化学方程式为
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.装置C中发生反应的离子方程式为
| ||
SO2+2OH-=SO32-+H2O
SO2+2OH-=SO32-+H2O
.(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是
试管A中气体压强减小,空气从D导管进入试管A中
试管A中气体压强减小,空气从D导管进入试管A中
.(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是
从D管口向A中通入空气(鼓气)
从D管口向A中通入空气(鼓气)
.【实验2】实验中发现试管内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜.
查阅资料:
①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜.
②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行如图的实验:
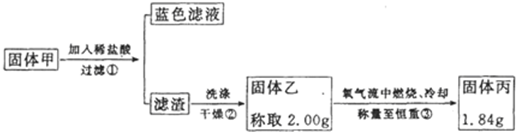
(4)②中检验滤渣是否洗涤干净的实验方法是
取最后一次洗涤后所得液体,滴加硝酸银溶液,若无白色沉淀产生,则说明沉淀洗涤干净;若有白色沉淀生成,则说明未洗干净
取最后一次洗涤后所得液体,滴加硝酸银溶液,若无白色沉淀产生,则说明沉淀洗涤干净;若有白色沉淀生成,则说明未洗干净
.(5)③中在煅烧过程中一定发生的反应的化学方程式为
2CuS+3O2
2CuO+2SO2
| ||
2CuS+3O2
2CuO+2SO2
.
| ||
(6)下列对于固体甲的成分的判断中,不正确的是(填字母选项)
BCD
BCD
.A.固体甲中,CuS和Cu2S不能同时存在
B.固体甲中,CuO和Cu2O至少有一种
C.固体甲中若没有Cu2O,则一定有Cu2S
D.固体甲中若存在Cu2O,也可能有Cu2S.
某气体由H2、CO2、CO、CH4中的两种组成,为确定其成分进行了下面的实验:
①取样,将气体通过灼热的氧化铜,有红色固体生成;
②另取样,将气体通过澄清的石灰水,未出现浑浊现象;
③另取样,将气体点燃后通入澄清的石灰水,有浑浊现象.
那么对该气体成分作出的以下推断中,不合理的是( )
①取样,将气体通过灼热的氧化铜,有红色固体生成;
②另取样,将气体通过澄清的石灰水,未出现浑浊现象;
③另取样,将气体点燃后通入澄清的石灰水,有浑浊现象.
那么对该气体成分作出的以下推断中,不合理的是( )
| A、H2、CO | B、CO2、CH4 | C、H2、CH4 | D、CO、CH4 |
丁烷在一定条件下裂解可按两种方式进行:
C4H10
C2H6+C2H4,C4H10
CH4+C3H6.
如图是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,省略)

按上图连好装置后,需进行的实验操作有:①给D、G装置加热; ②检查整套装置的气密性; ③排出装置中的空气等 …
(1)这三步操作的先后顺序依次是
(2)氧化铝的作用是
(3)B装置所起的作用是
(4)若对E装置中的混合物(溴水足量),再按以下流程实验:

①操作I、操作II分别是
②已知D的氢核磁共振谱图上只有一种峰,则D的结构简式

③Na2SO3溶液的作用是
(5)假定丁烷完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比n (CH4):n (C2H6)=
查看习题详情和答案>>
C4H10
| ||
| △ |
| ||
| △ |
如图是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,省略)

按上图连好装置后,需进行的实验操作有:①给D、G装置加热; ②检查整套装置的气密性; ③排出装置中的空气等 …
(1)这三步操作的先后顺序依次是
②、③、①
②、③、①
.(2)氧化铝的作用是
催化剂
催化剂
,写出甲烷与氧化铜反应的化学方程式CH4+4CuO
CO2+2H2O+4Cu
| △ |
CH4+4CuO
CO2+2H2O+4Cu
| △ |
(3)B装置所起的作用是
观察、控制丁烷气体的流速
观察、控制丁烷气体的流速
.(4)若对E装置中的混合物(溴水足量),再按以下流程实验:

①操作I、操作II分别是
分液
分液
、蒸馏
蒸馏
②已知D的氢核磁共振谱图上只有一种峰,则D的结构简式


③Na2SO3溶液的作用是
除去有机物中溶解的Br2
除去有机物中溶解的Br2
(5)假定丁烷完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比n (CH4):n (C2H6)=
1:1
1:1
(假定流经D、G装置中的气体能完全反应)某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质,首先做了银镜反应.
(1)在甲酸进行银镜反应前,必须在其中加入一定量的
(2)写出甲酸进行银镜反应的化学方程式:
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作
A、用洁净的试管;
B、在浓度为2%的NH3?H2O中滴入稍过量的浓度为2%的硝酸银;
C、用前几天配制好的银氨溶液;
D、在银氨溶液里加入稍过量的甲酸;
E、用小火对试管直接加热;
F、反应过程中,振荡试管使之充分反应.
然后,同学们对甲酸与甲醇进行了酯化反应的研究:
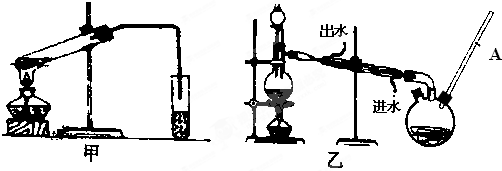
(4)乙装置中长导管A的作用是
(5)写出甲酸和甲醇进行酯化反应的化学方程式
(6)选择甲装置还是乙装置好?
(7)实验过程中选用的药品及试剂有:浓H2SO4、甲醇、甲酸还有
(8)一同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释
查看习题详情和答案>>
(1)在甲酸进行银镜反应前,必须在其中加入一定量的
NaOH(Na2CO3)溶液
NaOH(Na2CO3)溶液
,因为反应必须在碱性条件下发生
反应必须在碱性条件下发生
;(2)写出甲酸进行银镜反应的化学方程式:
HCOOH+2Ag(NH3)2OH
(NH4)2CO3+2Ag↓+2NH3↑+H2O
| △ |
HCOOH+2Ag(NH3)2OH
(NH4)2CO3+2Ag↓+2NH3↑+H2O
| △ |
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作
BCDEF
BCDEF
(写字母):A、用洁净的试管;
B、在浓度为2%的NH3?H2O中滴入稍过量的浓度为2%的硝酸银;
C、用前几天配制好的银氨溶液;
D、在银氨溶液里加入稍过量的甲酸;
E、用小火对试管直接加热;
F、反应过程中,振荡试管使之充分反应.
然后,同学们对甲酸与甲醇进行了酯化反应的研究:

(4)乙装置中长导管A的作用是
冷凝回流甲醇,平衡内外大气压强
冷凝回流甲醇,平衡内外大气压强
;(5)写出甲酸和甲醇进行酯化反应的化学方程式
HCOOH+CH3OH
HCOOCH3+H2O
| 浓硫酸 |
| △ |
HCOOH+CH3OH
HCOOCH3+H2O
| 浓硫酸 |
| △ |
(6)选择甲装置还是乙装置好?
乙
乙
,原因是冷凝效果好,减少了甲醇等有毒物质对大气的污染
冷凝效果好,减少了甲醇等有毒物质对大气的污染
;(7)实验过程中选用的药品及试剂有:浓H2SO4、甲醇、甲酸还有
饱和碳酸钠溶液
饱和碳酸钠溶液
、碎瓷片(沸石)
碎瓷片(沸石)
两种必备用品.(8)一同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释
强碱性条件下,甲酸甲酯水解了
强碱性条件下,甲酸甲酯水解了
.