摘要:10.工业上制取大量乙烯.丙烯所采用的方法是 ( C ) A.石油分馏 B.石油裂化 C.石油裂解 D.煤的干馏
网址:http://m.1010jiajiao.com/timu3_id_197024[举报]
 (1)食品和药品关系人的生存和健康.
(1)食品和药品关系人的生存和健康.①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是
A
A
(填字母).A.加钙盐 B.加碘盐 C.加锌盐
②碳酸镁可治疗胃酸过多的原理是
MgCO3+2H+=Mg2++CO2↑+H2O
MgCO3+2H+=Mg2++CO2↑+H2O
(用离子方程表示).③阿司匹林具有
解热镇痛
解热镇痛
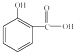
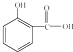
作用.长期大量服用阿司匹林,其水解产物水杨酸可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式:

(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活.
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点
低
低
(选填“高”或“低”).②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.铁锅的腐蚀主要是由
电化学腐蚀
电化学腐蚀
(填“化学腐蚀”或“电化学腐蚀”)造成的,铁锅锈蚀的负极电极反应式为Fe-2e-═Fe2+
Fe-2e-═Fe2+
.③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有CaCO3、
Na2CO3
Na2CO3
(填化学式)和SiO2.(3)防治环境污染,改善生态环境已成为全球的共识.
①pH<5.6的雨水称为酸雨,主要是由人为排放的硫氧化物和
氮氧化物
氮氧化物
等酸性气体转化而成的.向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2.发生反应的化学方程式为2CaCO3+O2+2SO2
2CaSO4+2CO2
| ||
2CaCO3+O2+2SO2
2CaSO4+2CO2
.
| ||
②城市餐饮业会产生大量污染环境的“地沟油”.综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和
高级脂肪酸
高级脂肪酸
.生活中会产生大量废弃塑料,将废弃塑料进行裂解
裂解
处理,可以获得乙烯、丙烯等化工原料.③含铬元素的废水必须治理达标.某兴趣小组探究含铬(Cr2O72ˉ)废水的处理方法,经查阅资料,拟采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3.该方案运用了污水处理方法中的氧化还原法和
沉淀法
沉淀法
.指导老师指出该方案处理后的废水中因含有大量NH4+
NH4+
(填离子符号),能导致水体富营养化.
工业上目前使用两种方法制取乙醛,即乙炔水化法和乙烯氧化法。下列两表提供了生产过程中所用原料、反应条件、原料平衡转化率、产量等有关的信息情况。
表一 原料、反应条件、平衡转化率、日产量
物质 项目 | 乙炔水化法 | 乙烯氧化法 |
原料 | 乙炔、水 | 乙烯、空气 |
反应条件 | HgSO4、100— | PdCl2—CuCl2、100— |
平衡转化率 | 乙炔平衡转化率90%左右 | 乙烯平衡转化率80%左右 |
日产量 | 2.5 t(某设备条件下) | 3.6 t(相同设备条件下) |
表二 原料来源生产工艺
反应过程 原料 | 原料生产工艺过程 |
乙炔 | CaCO3 |
乙烯 | 来源于石油裂解气 |
根据上述两表,完成下列问题:
(1)写出下列化学方程式。
a.乙炔水化法制乙醛:__________________。
b.乙烯氧化法制乙醛:__________________。
(2)从两表中分析,现代工业上乙烯氧化法逐步取代乙炔水化法,可能的原因(从环境、原料来源、产率和产量、能耗等角度):_____________________________________________。
(3)从化学反应速率角度分析,在相同条件下,两种制取乙醛的方法哪种快?
(4)若将上述两种方法的反应条件,均增加“100 atm”,原料平衡转化率_______ (填“增大”“减小”或“不变”)。而实际生产中不采用,理由是____________________________。
(5)若乙烯由石油裂化气(裂化气混合气体的平均分子式CnHm,m>2n),进一步完全催化裂解而来,得到体积分数分别为:甲烷,5%;乙烯,40%;丙烯,10%。其余为丁二烯和氢气(气体体积均在同温同压下测定)。若得到40 mol乙烯,求能够得到丁二烯和氢气各多少摩尔(用m、n代数式表示)。
查看习题详情和答案>>(1)食品和药品关系人的生存和健康.
①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是______(填字母).
A.加钙盐B.加碘盐C.加锌盐
②碳酸镁可治疗胃酸过多的原理是______(用离子方程表示).
③阿司匹林具有______作用.长期大量服用阿司匹林,其水解产物水杨酸可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式:______.
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活.
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点______(选填“高”或“低”).
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.铁锅的腐蚀主要是由______(填“化学腐蚀”或“电化学腐蚀”)造成的,铁锅锈蚀的负极电极反应式为______.
③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有CaCO3、______(填化学式)和SiO2.
(3)防治环境污染,改善生态环境已成为全球的共识.
①pH<5.6的雨水称为酸雨,主要是由人为排放的硫氧化物和______等酸性气体转化而成的.向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2.发生反应的化学方程式为______.
②城市餐饮业会产生大量污染环境的“地沟油”.综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和______.生活中会产生大量废弃塑料,将废弃塑料进行______处理,可以获得乙烯、丙烯等化工原料.
③含铬元素的废水必须治理达标.某兴趣小组探究含铬(Cr2O72ˉ)废水的处理方法,经查阅资料,拟采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3.该方案运用了污水处理方法中的氧化还原法和______.指导老师指出该方案处理后的废水中因含有大量______(填离子符号),能导致水体富营养化.
查看习题详情和答案>>
①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是______(填字母).
A.加钙盐B.加碘盐C.加锌盐
②碳酸镁可治疗胃酸过多的原理是______(用离子方程表示).
③阿司匹林具有______作用.长期大量服用阿司匹林,其水解产物水杨酸可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式:______.
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活.
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点______(选填“高”或“低”).
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.铁锅的腐蚀主要是由______(填“化学腐蚀”或“电化学腐蚀”)造成的,铁锅锈蚀的负极电极反应式为______.
③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有CaCO3、______(填化学式)和SiO2.
(3)防治环境污染,改善生态环境已成为全球的共识.
①pH<5.6的雨水称为酸雨,主要是由人为排放的硫氧化物和______等酸性气体转化而成的.向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2.发生反应的化学方程式为______.
②城市餐饮业会产生大量污染环境的“地沟油”.综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和______.生活中会产生大量废弃塑料,将废弃塑料进行______处理,可以获得乙烯、丙烯等化工原料.
③含铬元素的废水必须治理达标.某兴趣小组探究含铬(Cr2O72ˉ)废水的处理方法,经查阅资料,拟采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3.该方案运用了污水处理方法中的氧化还原法和______.指导老师指出该方案处理后的废水中因含有大量______(填离子符号),能导致水体富营养化.
