摘要: (2)反应速率慢 不利于晶体析出 Fe+2==3 (5)减小FeSO4的损失 防止空气进入试管将氧化为 (6)有浅绿色晶体析出
网址:http://m.1010jiajiao.com/timu3_id_196070[举报]
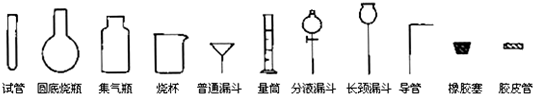
(2008?天津)Ⅰ.化学实验室制取气体的方法之一是将浓硫酸滴入浓盐酸中.请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图中标明所用试剂.(仪器可重复使用,固定装置不必画出)
Ⅱ.实验室制备少量硫酸亚铁品体的实验步骤如下:取过量洁净的铁屑,加入20%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口.静置、冷却一段时间后收集产品.
(1)写出该实验制备硫酸亚铁的化学方程式:
(2)硫酸溶液过稀会导致
(3)采用水浴加热的原因是
(4)反应时铁屑过量的目的是(用离子方程式表示)
(5)溶液趁热过滤的原因是
(6)静置冷却一段时间后,在试管中观察到的现象是
查看习题详情和答案>>

Ⅱ.实验室制备少量硫酸亚铁品体的实验步骤如下:取过量洁净的铁屑,加入20%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口.静置、冷却一段时间后收集产品.
(1)写出该实验制备硫酸亚铁的化学方程式:
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
.(2)硫酸溶液过稀会导致
反应速率慢 不利于晶体析出
反应速率慢 不利于晶体析出
.(3)采用水浴加热的原因是
容易控制温度
容易控制温度
.(4)反应时铁屑过量的目的是(用离子方程式表示)
Fe+2Fe3+═3Fe2+
Fe+2Fe3+═3Fe2+
.(5)溶液趁热过滤的原因是
减小FeSO4的损失
减小FeSO4的损失
.塞紧试管口的目的是防止空气进入试管将Fe2+氧化为Fe3+
防止空气进入试管将Fe2+氧化为Fe3+
.(6)静置冷却一段时间后,在试管中观察到的现象是
有浅绿色晶体析出
有浅绿色晶体析出
.