摘要:1].某反应的化学方程式为:aFeCl2十bKNO3+cHCl=dFeCl3+eKCI+fX+gH2O.若b=l.d=3.则X的化学式为 A N2 B NO C NO2 D NH4Cl
网址:http://m.1010jiajiao.com/timu3_id_194032[举报]
 在一定温度下,在容积为2L的容器内,某反应各物质(均为气体)的物质的量随反应时间的变化曲线如图,试回答下列问题:
在一定温度下,在容积为2L的容器内,某反应各物质(均为气体)的物质的量随反应时间的变化曲线如图,试回答下列问题:(1)该反应的化学方程式为
2N M
M
 M
M2N M
M
.? M
M(2)若t1=5S,则前5S用M表示的反应速率为
0.3mol/(L?s)
0.3mol/(L?s)
.(3)t2时,正反应速率
大于
大于
逆反应速率(填大于.等于或小于).(4)t3时若升高温度,则逆反应速率将
增大
增大
(填增大.减小或不变).(5)t3时减小容器的体积,则正反应率
大于
大于
逆反应速率(填大于、等于或小于). 某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:
某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:(1)①该反应的化学方程式是
2X 3Y+Z
3Y+Z
 3Y+Z
3Y+Z2X 3Y+Z
3Y+Z
. 3Y+Z
3Y+Z②在t1min时,该反应达到了
平衡
平衡
状态,下列可作为判断反应已达到该状态的是D
D
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为2:3
C.生成3mol Y的同时生成1mol Z
D.生成1mol Z的同时生成2mol X
(2)①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则至t1min时,该反应吸收的热量为:
36.8kJ
36.8kJ
;在此t1min时间内,用H2表示反应的平均速率v(H2)=| 0.6 |
| t1 |
| 0.6 |
| t1 |
②两位同学讨论放热反应和吸热反应.甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应.你认为他们说法正确的是
乙
乙
同学.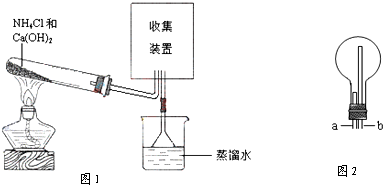 某兴趣小组同学用如图所示装置制取氨气并探究氨气的性质.
某兴趣小组同学用如图所示装置制取氨气并探究氨气的性质.请回答:
(1)图1试管中反应的化学方程式是
(2)用图2装置收集氨气时,进气口是
(3)向烧杯中滴加酚酞溶液,观察到溶液变红,说明
(4)将烧杯中的蒸馏水换成AlCl3溶液,当氨气进入烧杯后,观察到溶液中的现象是
某同学做Ca(OH)2溶液与Na2CO3溶液反应的实验:
(1)该反应的化学方程式是
(2)为使其反应完全,先向Ca(OH)2溶液中滴入几滴无色酚酞溶液,然后再滴入Na2CO3溶液.根据酚酞颜色的变化来判断反应是否完全进行,你认为这样做对不对?
查看习题详情和答案>>
(1)该反应的化学方程式是
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
.(2)为使其反应完全,先向Ca(OH)2溶液中滴入几滴无色酚酞溶液,然后再滴入Na2CO3溶液.根据酚酞颜色的变化来判断反应是否完全进行,你认为这样做对不对?
不对
不对
(填“对”或“不对”),理由是因为反应前Ca(OH)2溶液呈碱性,反应后生成的NaOH溶液也呈碱性,会使滴入的酚酞试液在反应前后始终呈红色
因为反应前Ca(OH)2溶液呈碱性,反应后生成的NaOH溶液也呈碱性,会使滴入的酚酞试液在反应前后始终呈红色
.一定温度下,某容积为2L的密闭容器内,某一反应中M(g)、N(g)的物质的量随反应时间变化的曲线如图,依图所示:
(1)该反应的化学方程式是
(2)在图上所示的三个时刻中,
态,此时V正
(3)下列描述中能说明上述反应达到平衡状态的是
A.容器中M与N的物质的量之比为1:1
B.混合气体的密度不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗2molN的同时生成1mol M
E.混合气体的压强不随时间的变化而变化
(4)下列措施能增大反应速率的是
A.升高温度 B.降低压强 C.减小M的浓度 D.将反应容器体积缩小.
查看习题详情和答案>>

(1)该反应的化学方程式是
2N (g) M (g)
M (g)
 M (g)
M (g)2N (g) M (g)
M (g)
. M (g)
M (g)(2)在图上所示的三个时刻中,
t3
t3
(填t1、t2或t3)时刻处于平衡状态,此时V正
=
=
V逆(填>、<或=,);达到平衡状态后,平均反应速率v(N)﹕v(M)=2:1
2:1
.(3)下列描述中能说明上述反应达到平衡状态的是
CE
CE
(填字母)A.容器中M与N的物质的量之比为1:1
B.混合气体的密度不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗2molN的同时生成1mol M
E.混合气体的压强不随时间的变化而变化
(4)下列措施能增大反应速率的是
AD
AD
(选填字母)A.升高温度 B.降低压强 C.减小M的浓度 D.将反应容器体积缩小.