摘要:将NaOH,MgCl2,AlCl3三种固体组成的混合物溶于足量水, 产生1.16g白色沉淀, 再向所得浊液中逐渐加入1.00 mol/L的盐酸, 加入盐酸的体积与生成沉淀的关系如下图: 请回答:①A点化学式 ,理由 ②写出A到B发生反应的离子方程式 ③原混合物中MgCl2质量是 g, AlCl3质量是 g, NaOH质量是 g ④C点消耗盐酸的体积为 答案:
网址:http://m.1010jiajiao.com/timu3_id_194010[举报]
将NaOH,MgCl2,AlCl3三种固体组成的混合物溶于足量水, 产生1.16g白色沉淀, 再向所得浊液中逐渐加入1.00 mol/L的盐酸, 加入盐酸的体积与生成沉淀的关系如下图:

请回答:①A点化学式____________,理由_______________
②写出A到B发生反应的离子方程式_______________________
③原混合物中MgCl2质量是_________g, AlCl3质量是_________g, NaOH质量是_________g
④C点消耗盐酸的体积为_______________
查看习题详情和答案>>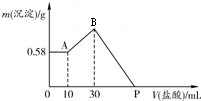 将NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得的浊液中,逐滴加0.4mol?L-1的盐酸,加入盐酸的体积和沉淀质量的变化关系如下图所示.下列说法错误的是( )
将NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得的浊液中,逐滴加0.4mol?L-1的盐酸,加入盐酸的体积和沉淀质量的变化关系如下图所示.下列说法错误的是( )| A、最初10 mL盐酸用于中和过量的NaOH溶液 | B、混合物中AlCl3的物质的量为0.008 mol | C、混合物中NaOH的质量为2.24 g | D、P点所示加入盐酸的体积为110 mL |