摘要:4. 硫化氢中含氯化氢和水:依次通过盛饱和NaHS的洗气瓶,盛五氧化二磷或无水氯化钙的干燥管
网址:http://m.1010jiajiao.com/timu3_id_193757[举报]
试回答下列问题:
某课外研究小组,用含有较多杂质的铜(主要杂质为Fe),通过下列化学反应制取胆矾并回收铁单质.请回答相关问题:

pH控制可参考下列数据:
(1)试剂A最好选用
加入试剂A以后,金属铜也能逐渐溶解,写出该反应的离子方程式
能否用稀硝酸代替试剂A
(2)Cu(OH)2的作用是
还可以用
(3)操作2中包含3个基本实验操作,依次为
(4)如何对操作1后所得滤渣进行洗涤?简述洗涤操作步骤
查看习题详情和答案>>
某课外研究小组,用含有较多杂质的铜(主要杂质为Fe),通过下列化学反应制取胆矾并回收铁单质.请回答相关问题:

pH控制可参考下列数据:
| 物 质 | 开始沉淀时的pH | 完全沉淀时的pH |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
a
a
(填字母);a.H2O2 b.氯水 c.酸性高锰酸钾加入试剂A以后,金属铜也能逐渐溶解,写出该反应的离子方程式
Cu+2H++H2O2═Cu2++2H2O
Cu+2H++H2O2═Cu2++2H2O
能否用稀硝酸代替试剂A
不能
不能
(填“能”或“不能”),原因是引入杂质NO3-并且会产生污染性气体NO
引入杂质NO3-并且会产生污染性气体NO
(2)Cu(OH)2的作用是
调节溶液的pH值,使Fe3+离子形成沉淀
调节溶液的pH值,使Fe3+离子形成沉淀
,还可以用
CuO
CuO
(填一种试剂)代替;不能
不能
(填“能”或“不能”)用NaOH溶液代替?(3)操作2中包含3个基本实验操作,依次为
蒸发浓缩
蒸发浓缩
、冷却结晶
冷却结晶
和过滤;操作1以后,加硫酸调节溶液的pH=1的目的是抑制Cu2+的水解
抑制Cu2+的水解
(4)如何对操作1后所得滤渣进行洗涤?简述洗涤操作步骤
过滤后,向漏斗缓缓中加入适量蒸馏水,使液面刚好没过滤渣,静置,待液体流下,重复操作2-3次
过滤后,向漏斗缓缓中加入适量蒸馏水,使液面刚好没过滤渣,静置,待液体流下,重复操作2-3次
.
某混合气体中可能含有氢气、一氧化碳、二氧化碳、氯化氢、氨气和水蒸气中的两种或几种,将混合气体依次通过:澄清石灰水(无浑浊现象)→氢氧化钡溶液(有浑浊现象)→浓硫酸(无明显现象)→灼热氧化铜(固体变红)→无水硫酸铜(固体变蓝).则混合气体中一定含有的成分是 .
查看习题详情和答案>>
(2013?奉贤区二模)综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如图所示:

完成下列填空
(1)实验室提纯粗盐的实验操作依次为:取样、
(2)气体X是
(3)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加
(4)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为
(5)由MgCl2?6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如下:

①上图中,装置a由
②循环物质甲的名称是
③制取无水氯化镁必须在氯化氢存在的条件下进行,主要原因是
④装置b中填充的物质可能是
e.硅胶 f.碱石灰 g. 无水氯化钙 h.浓硫酸
⑤方框中的d装置可选择

查看习题详情和答案>>

完成下列填空
(1)实验室提纯粗盐的实验操作依次为:取样、
溶解
溶解
、过滤
过滤
;加热浓缩、结晶
结晶
、过滤(或过滤;洗涤)
过滤(或过滤;洗涤)
、烘干.(2)气体X是
NH3
NH3
(填化学式),溶液II中发生反应的化学方程式是:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl
NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl
.(3)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加
HNO3、AgNO3
HNO3、AgNO3
.(4)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为
Cl2+2Br-═Br2+2Cl-
Cl2+2Br-═Br2+2Cl-
.(5)由MgCl2?6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如下:

①上图中,装置a由
圆底烧瓶
圆底烧瓶
、分液漏斗
分液漏斗
、双孔塞和导管组成②循环物质甲的名称是
盐酸
盐酸
,③制取无水氯化镁必须在氯化氢存在的条件下进行,主要原因是
抑止镁离子水解
抑止镁离子水解
,④装置b中填充的物质可能是
eg
eg
(填入编号)e.硅胶 f.碱石灰 g. 无水氯化钙 h.浓硫酸
⑤方框中的d装置可选择
AD
AD
.
“84消毒液”与硫酸溶液反应可以制取氯气(NaClO+ NaCl+H2SO4 Na2SO4 + Cl2↑+H2O)为探究氯气的性质,某同学设计了如下所示的实验装置
Na2SO4 + Cl2↑+H2O)为探究氯气的性质,某同学设计了如下所示的实验装置
 Na2SO4 + Cl2↑+H2O)为探究氯气的性质,某同学设计了如下所示的实验装置
Na2SO4 + Cl2↑+H2O)为探究氯气的性质,某同学设计了如下所示的实验装置 
请回答:
(1)从①、②、③装置中选择合适的制气装置(A处)__________(填写序号)。
(1)从①、②、③装置中选择合适的制气装置(A处)__________(填写序号)。

(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是__________,说明该装置存在明显的缺陷,请提出合理的改进的方法____________________。
(3)为了验证氯气的氧化性,将氯气通Na2SO3溶液中,写出氯气与Na2SO3溶液反应的离子方程式____________________
(4)氯气通入饱和NaHCO3溶液能产生无色气体,已知酸性盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有__________。
(5)写出氯气与氢氧化钠溶液反应的化学方程式____________________,为验证尾气吸收后的溶液中存在氯离子,正确的操作为____________________。
查看习题详情和答案>>
(3)为了验证氯气的氧化性,将氯气通Na2SO3溶液中,写出氯气与Na2SO3溶液反应的离子方程式____________________
(4)氯气通入饱和NaHCO3溶液能产生无色气体,已知酸性盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有__________。
(5)写出氯气与氢氧化钠溶液反应的化学方程式____________________,为验证尾气吸收后的溶液中存在氯离子,正确的操作为____________________。
“84消毒液”与硫酸溶液反应可以制取氯气(NaClO+ NaCl+H2SO4 ![]() Na2SO4 + Cl2↑+H2O)
Na2SO4 + Cl2↑+H2O)
为探究氯气的性质,某同学设计了如下所示的实验装置
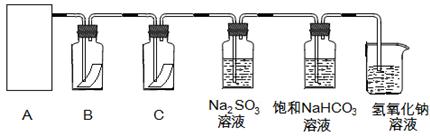
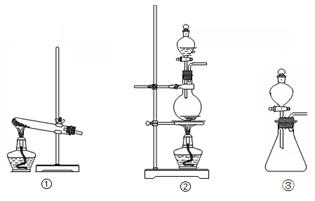
请回答:
(1)从①、②、③装置中选择合适的制气装置(A处) (填写序号)。
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是 ,说明该装置存在明显的缺陷,请提出合理的改进的方法 。
(3)为了验证氯气的氧化性,将氯气通Na2SO3溶液中,写出氯气与Na2SO3溶液反应的离子方程式 。
(4)氯气通入饱和NaHCO3溶液能产生无色气体,已知酸性盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有 。
(5)写出氯气与氢氧化钠溶液反应的化学方程式 ,为验证尾气吸收后的溶液中存在氯离子,正确的操作为 。
查看习题详情和答案>>