摘要:含极性共价键的离子化合物:碱.含氧酸盐.铵盐
网址:http://m.1010jiajiao.com/timu3_id_193746[举报]
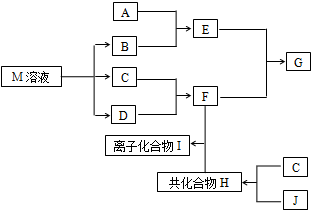
 短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:(1)X的离子结构示意图为




(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是
2Al+2NaOH+2H2O=2NaAlO2+3H2↑(或2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑)
2Al+2NaOH+2H2O=2NaAlO2+3H2↑(或2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑)
.(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是
SiO32-+2H+=H2SiO3↓
SiO32-+2H+=H2SiO3↓
.(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是
c(NH4+)>c(Cl-)>c(OH-)>c(H+)
c(NH4+)>c(Cl-)>c(OH-)>c(H+)
.(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
. 短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
(1)X的离子结构示意图为______;J的电子式是______.
(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是______.
(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是______.
(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是______.
(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为______.
查看习题详情和答案>>
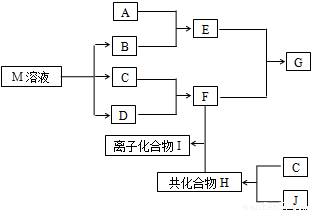
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
(1)X的离子结构示意图为______;J的电子式是______.
(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是______.
(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是______.
(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是______.
(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)X的离子结构示意图为______;J的电子式是______.
(2)若A是与X、Y同周期的一种常见金属单质,则A与B溶液反应的化学方程式是______.
(3)若A是一种常见酸性氧化物,且可用于制造玻璃,则E与F反应的离子方程式是______.
(4)将一定量F和H的水溶液混合使其溶液显碱性,则此溶液中离子浓度由大到小的顺序是______.
(5)汽油是一种可燃性液体,汽油-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,该电池放电时的正极反应式为______.
 查看习题详情和答案>>
查看习题详情和答案>>
(2011?德州一模)已知:短周期元素A、B、C、D、E原子序数依次增大.
(1)B、C、E三种元素组成的常见盐的水溶液呈酸性,原因是
(2)常温下,若甲、丙两溶液的pH均等于5,则由水电离出的c(H+)甲:c(H+)丙=
(3)盐丙中含有的化学键是
(4)0.1mol D单质和0.2mol E单质组成的混合物投入到足量的A2C中,产生气体的体积(标准状况)是
(5)反应:乙+C2→B2+A2C(未配平)可设计为燃料电池,则通入乙的电极是
(6)已知xC和yC是C元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是
A.xC2与yC2互为同分异构体
B.xC与yC核外电子排布方式不同
C.通过化学变化可以实现xC与yC间的相互转化
D.标准状况下,1.12L xC2和1.12L yC2均含有0.1NA个C原子.
查看习题详情和答案>>
| 元素代号 | 相关信息 |
| A | A与C可形成A2C和A2C2两种化合物 |
| B | B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D的单质能与冷水剧烈反应,得到强碱溶液 |
| E | 在第3周期元素中,E的简单离子半径最小 |
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
(用离子方程式表示).(2)常温下,若甲、丙两溶液的pH均等于5,则由水电离出的c(H+)甲:c(H+)丙=
10-4:1
10-4:1
;(3)盐丙中含有的化学键是
离子键、共价键
离子键、共价键
.(4)0.1mol D单质和0.2mol E单质组成的混合物投入到足量的A2C中,产生气体的体积(标准状况)是
4.48L
4.48L
.(5)反应:乙+C2→B2+A2C(未配平)可设计为燃料电池,则通入乙的电极是
负
负
极(填“正”或“负”),在碱性条件下其电极反应是2NH3+6OH--6e-=N2+6H2O
2NH3+6OH--6e-=N2+6H2O
.(6)已知xC和yC是C元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是
D
D
.A.xC2与yC2互为同分异构体
B.xC与yC核外电子排布方式不同
C.通过化学变化可以实现xC与yC间的相互转化
D.标准状况下,1.12L xC2和1.12L yC2均含有0.1NA个C原子.
下表是元素周期表的前三周期,针对表中A~G七种元素填空:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | | | | | | | |
| 2 | | | | B | C | D | | |
| 3 | E | | | | | F | G | |
(2)七种元素中的最高价氧化物对应水化物的酸性最强的是 (用化学式表示,下同);碱性最强的是 ,该化合物属于 。(选填离子或共价化合物),该化合物的电子式为 ,所含化学键类有 、 。
(3)用A、D的单质可以制成燃料电池,电池中装有E的最高价氧化物的水化物的浓溶液作电解质溶液,用多孔的金属惰性电极浸入上述浓溶液中,在X极通入D的单质,Y极通入A的单质,则Y极是该电池的 极(选填正极或者负极),X极的电极反应式是 。当电池中转移1 mol 电子时,消耗A单质的体积为 L(标况)。 查看习题详情和答案>>