摘要:电子得失守恒是指在发生氧化-还原反应时.氧化剂得到的电子数一定等于还原剂失去的电子数.无论是自发进行的氧化-还原反应还是原电池或电解池中均如此 [例题]将纯铁丝5.21克溶于过量稀盐酸中.在加热条件下.用2.53克KNO3去氧化溶液中亚铁离子.待反应后剩余的Fe2+离子尚需12毫升0.3摩/升KMnO4溶液才能完全氧化.写出硝酸钾和氯化亚铁完全反应的方程式 [分析]铁跟盐酸完全反应生成Fe2+.根据题意可知Fe2+分别跟KMnO4溶液和KNO3溶液发生氧化还原反应.KMnO4被还原为Mn2+.那么KNO3被还原的产物是什么呢? 根据电子得失守恒进行计算可得KNO3被还原的产物是NO. 所以硝酸钾和氯化亚铁完全反应的化学方程式为:
网址:http://m.1010jiajiao.com/timu3_id_193560[举报]
下列说法正确的是 ( )
| A.电解质是指在任何条件下均能导电的化合物 |
| B.NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质 |
| C.蔗糖、酒精在液态和水溶液里均不导电,所以它们是非电解质 |
| D.铜、石墨均导电,所以它们是电解质 |
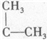 发生“烯烃复分解反应”,生成新烯烃种类为( )
发生“烯烃复分解反应”,生成新烯烃种类为( )