网址:http://m.1010jiajiao.com/timu3_id_193543[举报]
(1)下列各项符合“绿色化学”的要求的是
A.处理废弃物 B.治理污染点 C.减少有毒物 D.杜绝污染源
(2)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是
A.建在西部干旱区可以脱贫致富
B.应建在水资源丰富和交通方便的远离城市的郊区
C.企业有权自主选择厂址
D.不宜建在人口稠密的居民区
(3)某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+、Hg2+四种离子.甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案.

在能制得铜的方案中,哪一步操作会导致环境污染?
(4)CO2的含量增多时会造成“温室效应”,那么

仅限选择的仪器、用品和试剂:烧杯、试管、玻璃棒、胶头滴管、量筒、酒精灯、pH计、pH试纸;lmol/L盐酸、氯化氢气体、1mol/L氢氧化钠、lmol/L氯化铁、蒸馏水.
完成下列探究过程:
(1)写出FeCl3水解的离子方程式:
(2)针对FeCl3水解的影响因素提出假设:
假设 l:溶液的酸碱性;
假设 2:
假设 3:
(3)基于以上3个假设,设计出实验方案,将实验操作、预期的实验现象和结论填在下表中.
| 步骤编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入2mllmol/L氯化铁,观察溶液颜色,加热一段时间. 在试管中加入2mllmol/L氯化铁,观察溶液颜色,加热一段时间. |
加热后溶液颜色变深.说明升温促进氯铁水解, 生成更多的氢氧化铁胶体. 加热后溶液颜色变深.说明升温促进氯铁水解, 生成更多的氢氧化铁胶体. |
| ② | 在上述溶液中通入HCl气体 在上述溶液中通入HCl气体 |
上述溶液颜色变浅.说明加入酸使平衡左移,酸抑制氯化铁水解. 上述溶液颜色变浅.说明加入酸使平衡左移,酸抑制氯化铁水解. |
| ③ | 用量筒取10mllmol/L氯化铁于烧杯中,用pH计测出pH值.另取90ml蒸馏水加入烧杯,充分搅拌,再用pH计测出pH值. 用量筒取10mllmol/L氯化铁于烧杯中,用pH计测出pH值.另取90ml蒸馏水加入烧杯,充分搅拌,再用pH计测出pH值. |
前后测得pH值之差小于1.说明加水稀释后平衡右移,生成更多的H+.故增大氯化铁浓度,不利其水解. 前后测得pH值之差小于1.说明加水稀释后平衡右移,生成更多的H+.故增大氯化铁浓度,不利其水解. |
无 无 |
无 无 | |
| … | … | … |
(1)工业制溴如选择以上中的绿色氧化剂,其离子反应方程式为
(2)向FeCl3溶液通入SO2,能反应写化学方程式(不反应不填)
(3)将FeI2溶液与Cl2按物质的量之比为3:4完全反应的离子方程式为
(1)下列各项属于“绿色化学”的是( )
A.处理废弃物 B.治理污染点
C.减少有毒物 D.杜绝污染源
(2)在我国中西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是( )
A.建在中西部干旱山区可以脱贫致富
B.应建在水资源丰富和交通方便的远离城市的郊区
C.企业有权自主选择厂址
D.不宜建在人口稠密的居民区
(3)对聚丙烯酸废弃物(白色污染物中的一种)的降解,国际上最新采用了热聚门冬氨酸或其盐(TPA),它有效、廉价,且自身可被生物降解。废弃物自身被生物降解的意义是
________________________________________________________。
查看习题详情和答案>>早在20世纪90年代,国际上提出了“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各环节能都实现净化和无污染的反应途径。
(1)下列各项属于“绿色化学”的是 。
A.处理废弃物 B.治理污染点 C.减少有毒物 D.杜绝污染源
(2)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是 。
A.建在西部干旱区可以脱贫致富
B.应建在水资源丰富和交通方便的远离城市的郊区
C.企业有权自主选择厂址
D.不宜建在人口稠密的居民区
(3)坐落在山东沿海地区的潍坊纯碱厂是我国重点大型企业,其生产工艺沿用我国化学侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
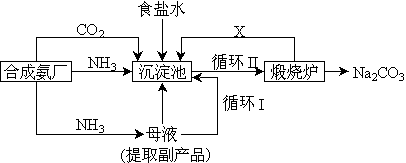
①上述生产纯碱的方法称 ,副产品的一种用途为 。
②沉淀池中发生的化学反应方程式是 。
③写出上述流程中X物质的分子式 。
④使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是 。
⑤母液中含有 ,(以化学式表示)。有向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 。
(a)增大NH4+的浓度,使NH4Cl更多地析出
(b)使NaHCO3更多地析出
(c)使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
查看习题详情和答案>>