网址:http://m.1010jiajiao.com/timu3_id_192932[举报]
某化工厂甲、乙两车间排放的废水中,分别含有较多量的Na2CO3和有毒物质CuSO4,两车间排放的废气中含有较多的SO2等有害气体。环保部门建议选用生石灰、铁屑和水等廉价易得的原料,综合治理上述污染,并回收得到铜和亚硫酸钠等有用物质。写出实现上述要求的化学方程式。(可不填满)
________________________________________________________________________;
________________________________________________________________________;
________________________________________________________________________;
________________________________________________________________________。
查看习题详情和答案>>
(1)甲厂的废水明显呈碱性,故甲厂的废水中所含的三种离子是:_________________。
(2)乙厂的废水含有另外三种离子,如果加一定量___________(选填:活性炭、FeSO4、铁粉),可以回收其中的金属_______________(填符号)。
另一种设想是将甲、乙两厂的废水按适当的比例混合,可以使废水中的_________________(填离子符号)转化为沉淀。经过滤后的废水主要含___________________,可用来浇灌农田。
查看习题详情和答案>>某中学环境监测兴趣小组的同学在一条鱼虾绝迹的小河边发现甲、乙、丙、丁四个工厂 ,如右图所示。这些工厂往小河里排放的废水中各含一种化合物。经检测发现:①甲处河水呈浅黄色;②乙处河水呈红褐色浑浊状;③丙处河水逐渐变澄清;④丁处河水不断冒气泡;⑤M处水样的pH大于7,加入足量的稀HNO3后再加入BaCl2溶液,无沉淀生成; ⑥N处水样的 pH小于7。请回答:
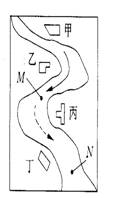
(1)四个工厂所排放的废水中,分别含有下列化合物中的哪种物质:
硫酸铁、氢氧化钠、硝酸银、碳酸钠、氯化铁、硫酸。
甲______, 乙______, 丙______, 丁______。(均填化学式)
(2)写出丙、丁两处所发生反应的离子方程式:
丙_______________ ; 丁_______________ 。
查看习题详情和答案>>
某中学环境监测兴趣小组的同学在一条鱼虾绝迹的小河边发现甲、乙、丙、丁四个工厂 ,如右图所示。这些工厂往小河里排放的废水中各含一种化合物。经检测发现:①甲处河水呈浅黄色;②乙处河水呈红褐色浑浊状;③丙处河水逐渐变澄清;④丁处河水不断冒气泡;⑤M处水样的pH大于7,加入足量的稀HNO3后再加入BaCl2溶液,无沉淀生成; ⑥N处水样的 pH小于7。请回答: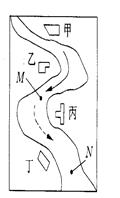
(1)四个工厂所排放的废水中,分别含有下列化合物中的哪种物质:
硫酸铁、氢氧化钠、硝酸银、碳酸钠、氯化铁、硫酸。
甲______, 乙______, 丙______, 丁______。(均填化学式)
(2)写出丙、丁两处所发生反应的离子方程式:
丙_______________ ; 丁_______________ 。
某中学环境监测兴趣小组的同学在一条鱼虾绝迹的小河边发现甲、乙、丙、丁四个工厂 ,如右图所示。这些工厂往小河里排放的废水中各含一种化合物。经检测发现:①甲处河水呈浅黄色;②乙处河水呈红褐色浑浊状;③丙处河水逐渐变澄清;④丁处河水不断冒气泡;⑤M处水样的pH大于7,加入足量的稀HNO3后再加入BaCl2溶液,无沉淀生成;⑥N处水样的 pH小于7。请回答:
(1)四个工厂所排放的废水中,分别含有下列化合物中的哪种物质:
硫酸铁、氢氧化钠、硝酸银、碳酸钠、氯化铁、硫酸。
甲______, 乙______, 丙______, 丁______。(均填化学式)
(2)写出丙、丁两处所发生反应的离子方程式:
丙_______________ ;丁_______________ 。
查看习题详情和答案>>