摘要:几点需要注意的问题: (1)常见的放热反应:①所有的燃烧反应②大多数的化合反应,(CO2+C2CO为吸热反应)③酸碱中和反应,④金属与酸或水反应置换出氢气⑤缓慢的氧化反应 (2)常见的吸热反应:①大多数的分解反应,②以下几个反应是吸热反应:Ba(OH)2·8H2O+2NH4Cl=2NH3↑+BaCl2+10H2O ,CO2+C2CO ,C+H2OCO+H2 注意:有热量放出未必是放热反应.放热反应和吸热反应必须是化学变化. 某些常见的热效应:(a)放热:①浓硫酸溶于水②NaOH溶于水③CaO溶于水.其中属于放热反应的是 .吸热:铵盐溶于水.(b)反应条件与热量变化没有必然的关系.既需要点燃或加热的反应不一定是吸热反应. 达标测试
网址:http://m.1010jiajiao.com/timu3_id_192804[举报]
在学习了原电池原理及应用后,张涛和李庆都有了以下收获:①凡是能自发进行的氧化还原反应都可以设计成原电池;②原电池中被腐蚀的一极为负极,负极的金属活动性大于正极金属等。两人均使用镁片与铝片作电极,分别设计了不同的原电池装置,结果却得到了关于镁、铝活动性相反的结论,你能想到他们设计的原电池有什么不同吗?由此,你是否想到利用原电池反应判断金属活动性顺序时还有哪些需要注意的问题?
查看习题详情和答案>>
(8分)碘化钠是无色立方晶体或白色结晶性粉末,具有还原性,可被一般氧化剂氧化。在医药上用作祛痰剂和利尿剂。也可用作照相胶片感光剂,碘的助溶剂。工业上用铁屑还原法来制备碘化钠,同时可得到副产品,该副产品常用作红色油漆和涂料。工艺流程如下: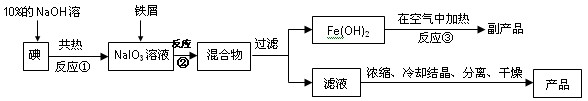
(1)反应①的还原产物为 ;反应②中的氧化剂是 。
(2)判断反应①中的碘是否已完全转化的具体操作方法是 。
(3)反应②的离子方程式为 ;
(4)将滤液浓缩、冷却、分离、干燥和包装过程中,都需要注意的问题是 。
碘化钠是无色立方晶体或白色结晶性粉末,具有还原性,可被一般氧化剂氧化。在医药上用作祛痰剂和利尿剂。也可用作照相胶片感光剂,碘的助溶剂。工业上用铁屑还原法来制备碘化钠,同时可得到副产品,该副产品常用作红色油漆和涂料。工艺流程如下:
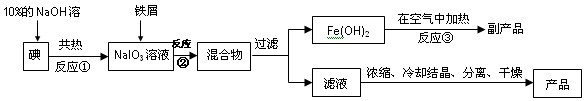
(1)反应①的还原产物为 ;反应②中的氧化剂是 。
(2)判断反应①中的碘是否已完全转化的具体操作方法是 。
(3)反应②的离子方程式为 ;
(4)将滤液浓缩、冷却、分离、干燥和包装过程中,都需要注意的问题是 。
查看习题详情和答案>>